De thi HSG 2018
Nội dung tài liệu
Tải xuống
Link tài liệu:
Các tài liệu liên quan
-
![48 câu trắc nghiệm Hóa học 9 chương 1]()
-
![Bảo toàn nguyên tố trong các bài toán vô cơ]()
-
![Bài tập phát triển năng lực ôn thi vào 10 chuyên Hóa và luyện thi HSG]()
-
![Các chuyên đề ôn thi học kì và tuyển sinh vào 10 Hóa 9]()
-
![Tuyển tập đề ôn thi HSG Hóa 9]()
-
![Các bài tập trắc nghiệm ôn thi học kì Hóa 9]()
-
![Chuyên đề Hóa 9: Kim loại]()
-
![458 câu trắc nghiệm ôn thi học kì 1 Hóa 9]()
-
![Một số câu hỏi thực tiễn chương trình Hóa 9]()
-
![Các chuyên đề ôn tập Hóa 9]()
Có thể bạn quan tâm
Thông tin tài liệu
TRƯỜNG THCS LƯƠNG THẾ VINH
Đề chính thức
ĐỀ THI CHỌN HỌC SINH GIỎI CẤP
TRƯỜNG
LỚP 9 TRUNG HỌC CƠ SỞ
Năm học 2018-2019 - Môn thi: HÓA HỌC
Thời gian : 150 phút (không kể phát đề)
Câu 1 (3,5 điểm).
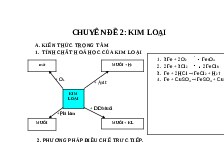
1. Viết các phương trình phản ứng để thực hiện chuỗi biến hóa sau:
FeCl3
Fe ( OH)3
FeCl2
FeSO4
Fe2O3
Fe
Fe(NO3)2
Fe(OH)2
2. Chỉ từ các chất: KMnO4, BaCl2, H2SO4 và Fe có thể điều chế được các khí gì?
Viết phương trình hóa học của các phản ứng tạo thành các khí đó.
Câu 2 (3,5 điểm).
1. Viết các phương trình phản ứng có thể xảy ra khi cho Al và Cl 2 lần lượt tác
dụng với H2O, dung dịch NaOH, dung dịch H 2SO4 loãng. Trong các phản ứng đó, phản
ứng nào có ứng dụng thực tế?
2. Cho 5,2 gam kim loại M tác dụng với axit H2SO4 loãng dư thu được 1,792 lít khí
H2 (ở đktc). Xác định kim loại M.
Câu 3 (4,5 điểm).
1. Không dùng thuốc thử nào khác hãy phân biệt các lọ dung dịch riêng bi ệt sau:
MgCl2, NaOH, NH4Cl, H2SO4, KCl.
2. Viết CTCT có thể có của hợp chất hữu cơ: C3H6; C2H6O.
Câu 4 (3,5 điểm). Hòa tan 7,83 gam một hỗn hợp gồm 2 kim loại kiềm A, B (nguyên tử
khối của A nhỏ hơn nguyên tử khối của B) thuộc 2 chu kì kế tiếp của bảng hệ thống
tuần hoàn các nguyên tố hóa học, thu được 2,8 lít khí H2 bay ra (điều kiện tiêu chuẩn).
1) Xác định kim loại A, B.
2) Cho 16,8 lit khí CO2 (điều kiện tiêu chuẩn) tác dụng hoàn toàn vào 600ml dung
dịch AOH 2M thu được dung dịch X. Tính tổng khối lượng muối trong dung dịch X.
Câu 5 (3,0 điểm). Hỗn hợp A1 gồm Al 2 O3 và Fe2 O3 . Dẫn khí CO qua 21,1 gam A1
và nung nóng thu được hỗn hợp A2 gồm 5 chất rắn và hỗn hợp khí A3 . Dẫn A3 qua
dung dịch Ca (OH ) 2 dư thấy có 5 gam kết tủa. A2 tác dụng vừa đủ với 1 lít dung dịch
H 2 SO4 0,5M thu được dung dịch A4 và có 2,24 lít khí thoát ra (đo ở đktc).
Tính % khối lượng mỗi chất trong hỗn hợp A1 .
Câu 6 (2,0 điểm). Cho 23,8 gam hỗn hợp X (Cu, Fe, Al) tác dụng vừa đủ 14,56 lít khí
Cl2 (đktc). Mặt khác cứ 0,25 Mol hỗn hợp tác dụng với dung dịch HCl d ư thu đ ược 0,2
Mol khí ( đktc). Tính phần trăm khối lượng mỗi kim loại trong hỗn hợp X.
Học sinh được sử dụng bảng hệ thống tuần hoàn các nguyên tố hóa học
- HẾT -
HƯỚNG DẪN CHẤM MÔN HÓA HỌC
Thi chọn học sinh giỏi cấp huyện lớp 9 THCS
Năm học 2018-2018
Nội dung
Câu
1.1
2,5
Điểm
2 Fe + 3 Cl2
FeCl3 + 3NaOH
Fe2 O3 + 3H2O
Fe + 2HCl
FeCl2 + H2
3 FeCl2
FeCl2 + Ag2 SO4
2,0
Điểm
2.1
1,5
Điểm
Fe (OH) 3+ 3NaCl
2Fe (OH) 3
2FeCl3 + Fe
1.2
2FeCl3
2 AgCl + FeSO4
FeSO4 + Ba ( NO3)2
Fe ( NO3)2 + Ba SO4
Fe ( NO3)2 +2NaOH
Fe (OH)2 + 2NaNO3
Có thể điều 0chế được các khí: O2, H2, SO2, HCl
t
2KMnO4 K2MnO4 + MnO2 + O2
H2SO4 loãng + Fe FeSO4 + H2
6H2SO4 (đặc, nóng) + 2Fe Fe2(SO4)3 + 6H2O + 3SO2
H2SO4 (đặc, nóng) + BaCl2 BaSO4 + 2HCl
Phương trình phản ứng:
2Al + 6H2O
2Al(OH)3↓ + 3H2↑
(0,25đ)
Cl2 + H2O
HCl + HClO (Điều chế nước clo)
(0,5 đ)
2Al + 3H2SO4
Al2(SO4)3 + 3H2↑
(0,25đ)
Cl2 + H2SO4 : không phản ứng
2Al + 2NaOH + 2H2O
2NaAlO2 + 3H2 (Điều chế H2)
(0,5đ)
NaCl + NaOCl + H 2O (Điều chế nước
Cl2 + 2NaOH
Javel)
2.2
2,0
Điểm
Gọi hoá trị của kim loại M là n . Ta có nH 2 =
= 0,08mol
2M + nH2SO4 M2(SO4)n + nH2
2.0,08
mol
n
Theo bài ra ta có:
n
M
3.1
2,5
Điểm
1,792
22,4
0,08mol
2.0,08
. M = 5,2 M = 32,5n . Ta có bảng sau:
n
1
2
3
32,loại)
65(Zn)
57,5 (loại)
Vậy nguyên tố cần tìm là Zn
Lấy mỗi lọ một ít dung dịch để làm mẫu thử, m ỗi l ần nh ỏ 1 dung
dịch vào mẫu thử của 4 dung dịch còn lại, sau 5 lần thí nghiệm các hi ện
tượng đươc ghi nhận vào bảng kết quả sau:
Điểm
0,25 đ
0,25 đ
0,25 đ
0,25 đ
0,25 đ
0,25 đ
0,25 đ
0,25 đ
0,25 đ
0,25 đ
0,25 đ
0,25 đ
0,25 đ
0,25 đ
0,25 đ
0,25 đ
0,25 đ
0,25 đ
0,25 đ
0,25 đ
Chất nhỏ
vào mẫu
thử
MgCl2
MgCl2
NaOH
NH4Cl
KCl
Mg(OH)2↓
Không
hiện
tượng
Không hiện
tượng
NH3↑
Không hiện
tương
NaOH
Mg(OH)2 ↓
NH4Cl
KCl
H2SO4
Không hiện
tượng
Không hiện
tương
Không hiện
tượng
Kết luận
1↓
H2SO4
Không hiện
tượng
NH3↑
Không
hiện
tượng
Không
hiện
tượng
1↓ , 1↑
Không
hiện
tượng
Không
hiện
tượng
1↑
Không
hiện
tượng
Không
hiện
tượng
Không
hiện
tượng
Không
hiện
tượng
Không hiện
tượng
* Kết quả:
- Tạo kết tủa trắng, mẫu thử đó là MgCl2.
(0,25đ)
- Tạo kết tủa trắng và khí có mùi khai bay ra, mẫu thử đó là NaOH.
(0,25đ)
- Tạo khí có mùi khai, mẫu thử đó là NH4Cl.
(0,25đ)
- Còn 2 mẫu thử không có hiện tượng, lấy kết tủa Mg(OH) 2 cho vào, mẫu
thử nào làm tan kết tủa là H2SO4.
(0,25đ)
- Mẫu còn lại là KCl.
(0,25đ)
* Các phương trình phản ứng:
MgCl2 + 2NaOH
Mg(OH) 2↓ + 2NaCl
(0,25đ)
NH4Cl +
NaOH
(0,25đ)
Mg(OH)2 + H2SO4
NaCl
+
NH 3↑ +
H2O
MgSO4 + 2H2O
* Nhận biết được 1 chất kèm biện luận đầy đủ được 0,5 điểm
3.2
4
3,5
điểm
Mỗi CTPT viết đủ 2 CTCT, mỗi CTCT được 0,5 điểm
2,0 điểm
4.1
Đặt M là nguyên tử khối trung bình của A, B => MA < M < MB
2A + 2 H2O
a mol
2AOH +
0,25 đ
H 2↑
a mol
a
mol
2
0,25 đ
(0,5đ)
2B + 2 H2O
2BOH +
H 2↑
b mol
0,25 đ
b mol
b
mol
0,25 đ
2
(0,5đ)
a +b 2,8
=
=
2
22, 4
nH 2
0,25 đ
=> a + b = 0,25
0,25 đ
(0,25đ)
7,83
M = 0, 25 = 31,32 => MA < 31,32 < MB
0,25 đ
(0,25đ)
Theo đề bài A, B là kim loại kiềm thuộc 2 chu kì kế tiếp suy ra:
A là Na ( MNa = 23) và B là K ( MK = 39).
(0,5đ)
0,25 đ
0,25 đ
4.2
16,8
nCO2 =
=0, 75 mol
22, 4
0,25 đ
0,25 đ
(0,25đ)
0,25 đ
nNaOH =CM ´ V =2 ´ 0, 6 =1, 2 mol
(0,25đ)
Vì nCO ánNaOH á2nCO do đó thu được hỗn hợp 2 muối:
CO2
+
2NaOH
Na 2CO3 + H2O
(1) 0,25 đ
(0,25đ)
x mol
2x mol
CO2
+
NaOH
(2)
2
0,25 đ
2
x mol
NaHCO 3
(0,25đ)
y mol
y mol
y mol
Gọi : x mol là số mol của Na2CO3
y mol là số mol của NaHCO3
nCO2 =x +y =0, 75 mol
(0,25đ)
nNaOH =2 x +y =1, 2 mol
(0,25đ)
ì x =0, 45
Þ í
î y =0,3
(0,25đ)
Þ mNa2CO3 =0, 45 ´ 106 =47, 7 gam
(0,25đ)
mNaHCO3 =0,3 ´ 84 =25, 2 gam
(0,25đ)
Tổng khối lượng muối trong dung dịch A:
m =mNa2CO3 +mNaHCO3 =72,9 gam
5
3,0
điểm
Gọi số mol của Al 2 O3 và Fe 2 O3 trong A1 lần lượt là a và b . (a 0; b 0). Số
mol oxi nguyên tử trong A1 là: nO 3a 3b
Theo giả thiết ta tính được: n H 2 SO4 1.0,5 0,5(mol ).
Các phản ứng có thể xảy ra:
3Fe2 O3 CO t 2 Fe3 O4 CO2
(1)
t
Fe3 O4 CO 3FeO CO2
(2)
t
FeO CO Fe CO2
(3)
CO2 Ca(OH ) 2( du ) CaCO3 H 2 O
(4)
o
o
o
5
nCO2 nCaCO3
0,05(mol )
100
A2 gồm: Al 2 O3 ; Fe 2 O3 ; Fe3 O4 ; FeO ; Fe . Khí A3 là CO và CO2 ; A2 tác
dụng với dung dịch H 2 SO4 loãng thu được khí đó là khí H 2
Oxit H 2 SO4 H 2 O Muối
(5)
0,4
nH2
0,25 đ
0,5 đ
0,25 đ
0,25 đ
0,25 đ
(mol)
(6)
Fe H 2 SO4 FeSO4 H 2
0,1
0,25 đ
0,1
0,25 đ
(mol)
2,24
0,1( mol ) . Số mol nguyên tử oxi trong A1 bằng tổng số mol nguyên
22,4
tử oxi trong A2 và số mol nguyên tử oxi chuyển từ CO thành CO2 (hay số mol
CO2 ). Mà số mol nguyên tử oxi trong A2 bằng số mol H 2 SO4 đã phản ứng
trong (5). Mà n H 2 SO4 (5) n H 2 SO4 (bandau) n H 2 SO4 ( 6) n H 2 SO4 ( bandau) n H 2 ( 6)
Do vậy ta có phương trình:
3a + 3b = 0,5 - n H 2 ( 6 ) + 0,05 3a + 3b = 0,5 – 0,1 + 0,05 = 0,45
(I)
Mặt khác: m hỗn hợp = 102a + 160b = 21,1
(II)
Giải (I) và (II) ta thu được nghiệm: a = 0,05; b = 0,1
0,25 đ
0,25 đ
0,25 đ
0,25 đ
6
2,0
điểm
Các phương trình phản ứng.
Cu + Cl2 →CuCl2
0,25 đ
(1)
(2)
(3)
2Fe + 3Cl2 → 2FeCl3
2Al + 3Cl2 → 2AlCl3
Fe + 2HCl → FeCl2 + H2
2Al + 6HCl → 2AlCl3 + 3H2 (5)
0,25 đ
(4)
Gọi a, b, c lần lượt là số mol của Cu, Fe, Al
Khối lượng hỗn hợp:
64a+56b+27c = 23,8
Theo (1), (2), (3) số mol clo:
a+ 3b/ 2 +3c/2 = 0,65
(II)
Vì số số mol X tỉ lệ với số mol khí hidro thu được :
0,2 (a+b+c) = 0,25 (b+ 3/2c)
Kết hợp (I), (II), (III) giải ta được:
Giải hệ: a =0,2 (%Cu=53,78)
b = 0,1(%Fe = 23,53)
c = 0,2(22,69)
0,25 đ
(I)
0,25 đ
0,25 đ
(III)
0,5 đ
0,25 đ