De on HSG 9
Nội dung tài liệu
Tải xuống
Link tài liệu:
Các tài liệu liên quan
-
![48 câu trắc nghiệm Hóa học 9 chương 1]()
-
![Bảo toàn nguyên tố trong các bài toán vô cơ]()
-
![Bài tập phát triển năng lực ôn thi vào 10 chuyên Hóa và luyện thi HSG]()
-
![Các chuyên đề ôn thi học kì và tuyển sinh vào 10 Hóa 9]()
-
![Tuyển tập đề ôn thi HSG Hóa 9]()
-
![Các bài tập trắc nghiệm ôn thi học kì Hóa 9]()
-
![Chuyên đề Hóa 9: Kim loại]()
-
![458 câu trắc nghiệm ôn thi học kì 1 Hóa 9]()
-
![Một số câu hỏi thực tiễn chương trình Hóa 9]()
-
![Các chuyên đề ôn tập Hóa 9]()
Có thể bạn quan tâm
Thông tin tài liệu
ĐỀ THI CHỌN HỌC SINH GIỎI LỚP 9
Năm học: 2011 – 2012
Môn: Hoá Học
( Thời gian 150 phút không kể thời gian giao đề)
Trêng THCS §an Hµ
Câu 1 ( 3 điểm)
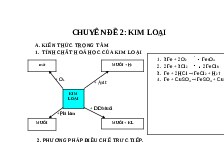
1. Hoàn thành sơ đồ chuyển hoá sau, xác định rõ các chất ứng với kí hiệu A, B, C, D,
E, F, G. ( A, B, C, D, E, F, G là các chất vô cơ)
Fe(nóng đỏ) + O2 A
A + HCl B + C + H2O
B + NaOH D + G
C + NaOH E + G
D + O2 + H2O E
E F + H2O
2. Cho kim loại Natri vào dung dịch hai muối Al2(SO4)3 và CuSO4 thì thu được
khí A, dung dịch B và kết tủa C. Nung kết tủa C được chất rắn D. Cho hiđrô
dư đi qua D nung nóng được chất rắn E. Hoà tan E vào dung d ịch HCl d ư th ấy
E tan một phần. Giải thích và viết phương trình hoá học các phản ứng.
Câu 2 ( 3 điểm)
1.Chọn các chất X, Y, Z, T thích hợp và viết các phương trình hoá h ọc hoàn
thành sơ đồ biến hoá sau:
t0
(1)
X
(2)
Y
FeSO4
(4)
FeCl2
(5)
Fe(NO3)2
(6)
X
(7)
T
(8)
Z
(3)
Z
2. Chỉ dùng một thuốc thử duy nhất, hãy nhận biết các dung dịch mất nhãn:
NH4Cl, MgCl2; FeCl2; AlCl3. Viết các phương trình phản ứng xảy ra.
Câu 3 ( 2 điểm)
Hoà tan 3,2 gam oxit của một kim loại hoá trị ( III) b ằng 200 gam dung d ịch
H2SO4 loãng. Khi thêm vào hỗn hợp sau phản ứng một lượng CaCO 3 vừa đủ
thấy thoát ra 0,224 dm3 CO2 (đktc), sau đó cô cạn dung dịch thu được 9,36 gam
muối khan. Xác định oxit kim loại trên và nồng độ % H2SO4 đã dùng.
Câu 4 ( 2 điểm)
Đốt m gam bột sắt trong khí oxi thu được 7,36 gam chất rắn X gồm: Fe;
FeO; Fe3O4; Fe2O3. Để hoà tan hoàn toàn hỗn hợp X cần vừa hết 120 ml dung
dịch H2SO4 1M ( loãng), tạo thành 0,224 l H2 ở đktc.
a. Viết phương trình hoá học xảy ra.
b. Tính m?
Cho Fe = 56, O = 16, Ca = 40, S = 32, C = 12, H = 1
1
Trêng THCS §an Hµ
Híng dÉn chÊm THI CHỌN HỌC SINH GIỎI LỚP
9
Năm học: 2011 – 2012
Môn: Hoá Học
Nội dung
Câu
1.
t
3Fe + 2O2 ¾¾
® Fe3O4
(A)
Fe3O4 + 8HCl → FeCl2 + 2FeCl3 + 4H2O
(A)
(B)
(C)
FeCl2 + 2NaOH → Fe(OH)2 + 2NaCl
(B)
(D)
(G)
FeCl3 + 3NaOH → Fe(OH)3 + 3NaCl
(C)
(E)
(G)
4Fe(OH)2 + O2 + H2O → 4Fe(OH)3
(D)
(E)
t
2Fe(OH)3 ¾¾® Fe2O3 + 3H2O
(E)
(F)
0
0
1
Điểm
(3 điểm)
0,25đ
0,25đ
0,25đ
0,25đ
0,25đ
0,25đ
2:- Khi cho Na vào 2 muối Na sẽ phản ứng với nước
trong dung dịch trước.
0,25đ
2 Na + 2 H2O
2 NaOH + H2
Sau đó dd NaOH sẽ có phản ứng:
6 NaOH + Al2(SO4)3
2Al(OH)3 + 3Na2SO4
0,25đ
NaOH + Al(OH)3
NaAlO2 + 2 H2O
2 NaOH + CuSO4
Cu(OH)2 + Na2SO4
Vậy Khí A là H2
- Dung dịch B là: NaAlO2 và Na2SO4
0,25đ
- Kết tủa C là Cu(OH)2 và Al(OH)3 chưa phản ứng hết.
Nung kết tủa C:
to
Cu(OH)2
CuO + H2O
o
t
2 Al(OH)3
Al2O3 + 3 H2O
0,25đ
- Chất rắn D là: Al2O3 và CuO.
- Cho hiđro dư qua D nung nóng,chỉ có CuO tham gia
0,25đ
khử:
to
CuO + H2
Cu + H2O
- Vậy rắn E là Cu Và Al2O3 ( không có CuO vì H2 dư)
Hoà tan E vào HCl, E tan một phần vì Cu không phản
2
ứng với HCl.
Al2O3 + 6 HCl
0,25đ
2 AlCl3 + 3 H2O
(3 điểm)
2
1. X là Fe(OH)2
Z là Fe
Y là Fe3O4
T là FeO
2 điểm
Phương trình phản ứng:
Viết
1/ Fe(OH)2 + H2SO4
FeSO4 + 2 H2O
đúng
2/ Fe3O4 + 4 H2SO4
FeSO4 + Fe2(SO4)3 + 4 H2O mỗi
3/ Fe + H2SO4
FeSO4 + H2
PTHH
4/ FeSO4 + BaCl2
FeCl2 + BaSO4
được
5/ FeCl2 + 2 AgNO3
Fe(NO3)2 + 2 AgCl
0,25đ
6/ Fe(NO3)2 +2 NaOH
Fe(OH)2 + 2 NaNO3
t
7/ Fe(OH)2 ¾¾® FeO + H2O
t
8/ FeO + CO ¾¾
® Fe + CO2
1 điểm
2. Nhận biết
- Dùng NaOH để nhận biết các dung dịch.
0,25đ
+ DD nào có khí mùi khai ( NH3) bay ra là NH4Cl.
NaOH + NH4Cl
NaCl + NH3() + H2O
0,25đ
+ DD nào có kết tủa trắng (Mg(OH)2) là MgCl2.
2 NaOH + MgCl2
Mg(OH)2 + 2 NaCl
+ DD nào có kết tủa trắng xanh sau hoá nâu ngoài không
Khí là FeCl2.
0,25đ
2 NaOH + FeCl2
Fe(OH)2 + 2 NaCl
4 Fe(OH)2 + O2 + 2 H2O
4 Fe(OH)3
+ DD nào xuất hiện kết tủa keo trắng, tan khi NaOH
dư là AlCl3
0,25đ
3 NaOH + AlCl3
Al(OH)3 + 3 NaCl
NaOH dư + Al(OH)3
NaAlO2 + 2 H2O
Gọi công thức của oxit là A2O3
( 2điểm)
A2O3 + 3 H2SO4
A2(SO4)3 + 3 H2O (1)
0,02
0,06 mol
0,25đ
H2SO4 dư + CaCO3
CaSO4 + H2O + CO2 (2)
1.
số mol CO2 = 0,01 mol
theo pt (2) Số mol H2SO4 dư = số mol CO2 = số mol 0,25đ
CaSO4 = 0,01 mol
Dd khi cô cạn có 9,36 gam muối khan
0,25đ
m A 2 (SO 4 ) 3 + mCaSO4 = 9,36
0
0
3
mA (SO )
m A (SO
2
4
+ 0,01. 136 = 9,36
3
= 9,36 – 1,36 = 8 g
theo (1) số mol A2O3 = số mol A2(SO4)3
3,2
_
8
2
4
)3
0,25đ
3
2 MA + 48
2 MA + 288
Giải ra ta được MA = 56. Vậy oxit là Fe2O3
0,25đ
2.
Theo PT (1) ta có số mol của Fe2O3 = 3,2/160 = 0,02 0,25đ
số mol H2SO4 ở (1) là 0,02.3 = 0.06 mol
tổng số mol H2SO4 ở (1) và (2) là 0,01 + 0,06 = 0,07
0,25đ
Khối lượng H2SO4 = 6,86 g
Nồng độ % là: 3,43 %.
0,25đ
( 2điểm)
Các PTHH:
t
2 Fe + O2 ¾¾
® 2 FeO
t
3 Fe + 2 O2 ¾¾® Fe3O4
t
4 Fe + 3 O2 ¾¾
® 2 Fe2O3
Fe + H2SO4
FeSO4 + H2
(1)
FeO + H2SO4
FeSO4 + H2O (2)
Fe3O4 + 4H2SO4 → FeSO4 + Fe2(SO4)3+ 4H2O (3)
Fe2O3 + 3 H2SO4 → Fe2(SO4)3+ 3 H2O
(4)
Số mol khí H2 sinh ra sau phản ứng là: 0,01 mol
Khối lượng Fe trong hỗn hợp X là:
Theo (1) số mol Fe = số mol H2 sinh ra = 0,01 mol = số
Mol H2SO4 ở (1)
khối lượng của Fe l à: 0,01. 56 = 0,56 g
Số mol H2SO4 phản ứng ở (2), (3), (4) l à
0,12.1 – 0,01 = 0,11 mol
Cũng theo (2), (3), (4) ta thấy:
Số mol H2SO4 = số mol nước = số mol oxi trong hỗn
hợp các oxit = 0,11 mol
Khối lượng của nguyên tử oxi trong oxit là:
0,11.16 = 1,76 g
Áp dụng ĐLBTNT: khối lượng của Fe = Khối lượng
của oxit - khối lượng của oxi
7,36 – 1,76 = 5,6 g
0
0
0
4
(0,5đ)
0,25đ
0,25đ
0,25đ
0,25đ
0,5đ
4