Bài 5: Luyện tập về axit-bazo-muối; phản ứng trao đổi ion trong dung dịch chất điện li.
Bài tập trắc nghiệm 1.37 trang 8 sách bài tập(SBT) hóa học 11
Một mẫu nước mưa có pH = 4,82. Vậy nồng độ H+ trong đó là :
A. [H+] = 1.10-4M.
B. [H+] = 1.10-5M.
C. [H+] > 1.10-5M.
D. [H+] < 1.10-5M.
Hướng dẫn giải
Đáp án C
Bài tập trắc nghiệm 1.38, 1.39, 1.40 trang 9 sách bài tập(SBT) hóa học 11
1.38. Dung dịch axit mạnh một nấc X nồng độ 0,01 mol/l có pH = 2 và dung dịch bazơ mạnh một nấc Y nồng độ 0,01 mol/l có pH = 12. Vậy :
A. X và Y là các chất điện li mạnh.
B. X và Y là các chất điện li yếu.
C. X là chất điện li mạnh, Y là chất điện li yếu.
D. X là chất điện li yếu, Y là chất điện li mạnh.
1.39. Dung dịch axit mạnh \({H_2}S{O_4}\) 0,1M có :
A. pH = 1.
B. pH < 1.
C. pH > 1.
D. [H+] > 0,2M.
1.40. Có V lít dung dịch NaOH 0,6M. Những trường hợp nào dưới đây làm pH của dung dịch NaOH đó giảm xuống ?
1. Thêm V lít nước cất.
2. Thêm V lít dung dịch KOH 0,67M.
3. Thêm V lít dung dịch HCl 0,3M.
4. Thêm V lít dung dịch NaN03 0,4M.
Hướng dẫn giải
1.38. A
1.39. B
1.40. Các trường hợp 1, 3 và 4.
Bài tập 1.41 trang 9 sách bài tập(SBT) hóa học 11
Nồng độ H+ trong rượu vang là 3,2.10-4M. Sau khi mở nút chai để hở trong không khí một tháng, nồng độ H+ là 1.10-3M. Hỏi pH của rượu vang tăng lên hay giảm xuống sau khi để trong không khí ?
Hướng dẫn giải
Giảm xuống.
Bài tập 1.42 trang 9 sách bài tập(SBT) hóa học 11
Viết phương trình dạng phân tử ứng với phương trình ion rút gọn sau :
1. Ba2+ + C\({O_3}^{2 - }\) \( \to \) BaC03\( \downarrow \)
2. Fe3+ + 3O\({H^ - }\) \( \to \) Fe(OH)3\( \downarrow \)
3. N\({H^{4 + }}\) + O\({H^ - }\) \( \to \) NH3\( \uparrow \) +H20
4. \({S^{2 - }}\) + 2H+ \( \to \) H2S\( \uparrow \)
5. HClO + O\({H^ - }\) \( \to \) Cl\({O^ - }\) + H20
6. C02 + 2O\({H^ - }\) \( \to \) C\({O_3}^{2 - }\) + H20
Hướng dẫn giải
1. \(BaS{O_4} + N{a_2}C{O_3} \to \)\(BaC{O_3} + N{a_2}S{O_4}\)
2. \(2FeC{l_3} + 3Ba{\left( {OH} \right)_2} \to \)\(2Fe{\left( {OH} \right)_3} + 3BaC{l_2}\)
3. \({(N{H_4})_2}S{O_4} + 2KOH \to \)\(2N{H_3} + 2{H_2}O + {K_2}S{O_4}\)
4. \(FeS + 2HCl \to \)\({H_2}S + FeC{l_2}\)
5. \(NaOH + HClO \to NaClO + {H_2}O\)
6. \(C{O_2} + 2NaOH \to N{a_2}C{O_3} + {H_2}O\)
Bài tập 1.43 trang 9 sách bài tập(SBT) hóa học 11
Viết phương trình dạng phân tử và ion rút gọn của các phản ứng trong dung dịch theo sơ đồ sau :
1. Pb(N03)2 + ? \( \to \) PbCl2\( \downarrow \) + ?
2. Sn(OH)2 + ? \( \to \) Na2Sn02\( \downarrow \) + ?
3. MgC03 + ? \( \to \) MgCl2 + ?
4. \(HP{O_4}^{2 - }\) + ? \( \to \) \({H_3}P{O_4}\) + ?
5. FeS + ? \( \to \) FeCl2 + ?
6. \(F{e_2}{(S{O_4})_3}\) + ? \( \to \) K2S04 + ?
Hướng dẫn giải
1. \(Pb{(N{O_3})_2} + 2KCl \to PbC{l_2} + 2KN{O_3}\)
2. \(Sn{(OH)_2} + 2NaOH \to N{a_2}Sn{O_2} + 2{H_2}O\)
3. \(MgC{O_3} + 2HCl \to MgC{l_2} + C{O_2} + {H_2}O\)
4. \(CaHP{O_4} + 2HN{O_3} \to {H_3}P{O_4} + Ca{(N{O_3})_2}\)
5. \(F{\rm{e}}S + 2HCl \to FeC{l_2} + {H_2}S\)
6. \(F{e_2}{(S{O_4})_3} + 6KI \to 3{K_2}S{O_4} + 2FeC{l_2} + {I_2}\)
Bài tập 1.44 trang 10 sách bài tập(SBT) hóa học 11
Hoà tan hoàn toàn 0,12 g Mg trong 100 ml dung dịch HCl 0,2M. Tính pH của dung dịch sau khi phản ứng kết thúc (thể tích dung dịch biến đổi không đáng kể).
Hướng dẫn giải
nMg = \(\frac{{0,12}}{{24}}\) = 0,005 (mol); nHCl = \(\frac{{0,2.100}}{{1000}}\) = 0,02 (mol)
Mg + 2HCl \( \to \) MgCl2 + H2
1 mol 2 mol
0,005 mol 0,01 mol
Số mol HCl còn lại sau phản ứng : 0,02 - 0,01 = 0,01 (mol).
Từ đó, số mol HCl trong 1000 ml là 0,1 mol, nghĩa là sau phản ứng
[HCl] = 0,1M = \({1.10^{ - 1}}\)M.
Vậy pH= 1.
Bài tập 1.45 trang 10 sách bài tập(SBT) hóa học 11
Trong nước biển, magie là kim loại có hàm lượng lớn thứ hai sau natri. Mỗi kilogam nước biển chứa khoảng 1,3 g magie dưới dạng các ion Mg2+. Ở nhiều quốc gia, magie được khai thác từ nước biển. Quá trình sản xuất magie từ nước biển gồm các giai đoạn sau :
1. Nung đá vôi thành vôi sống.
2. Hoà tan vôi sống trong nước biển tạo ra kết tủa Mg(OH)2.
3. Hoà tan kết tủa Mg(OH)2 trong dung dịch HCl.
4. Điện phân MgCl2 nóng chảy : MgCl2 ![]() Mg + Cl2
Mg + Cl2
Viết các phương trình hoá học dưới dạng phân tử và ion rút gọn (nếu có) của quá trình sản xuất trên.
Hướng dẫn giải
1. CaC03 ![]() CaO + C02\( \uparrow \)
CaO + C02\( \uparrow \)
2. CaO + H20 \( \to \) Ca(OH)2
Mg2+ + 2O\({H^ - }\) \( \to \) Mg(OH)2
3. Mg(OH)2 + 2HCl \( \to \) MgCl2 + 2H20
Mg(OH)2 + 2H+ \( \to \) Mg2+ + 2H20
4. MgCl2 ![]() Mg + Cl2
Mg + Cl2
Bài tập 1.46 trang 10 sách bài tập(SBT) hóa học 11
Nước chứa nhiểu ion Ca2+ và Mg2+ là nước cứng. Nước chứa ít hoặc không chứa các ion Ca2+ và Mg2+ là nước mềm. Nước cứng không phù hợp cho việc sử dụng trong công nghiệp và sinh hoạt. Trong nước thường chứa các hợp chất Ca(HC03)2, Mg(HC03)2, CaCl2 và MgCl2 hoà tan.
Để loại các ion Ca2+ và Mg2+ dưới dạng Ca(HC03)2, Mg(HC03)2 và MgCl2 người ta cho sữa vôi Ca(OH)2 vào nước sẽ tạo ra các kết tủa CaC03 va Mg(OH)2.
Để loại Ca2+ dưới dạng CaCl2 người ta hoà tan Na2C03 vào nước sẽ tạo kết tủa CaC03.
Hãy viết các phương trình hoá học dưới dạng phân tử và ion rút gọn của các phản ứng trên.
Hướng dẫn giải
Ca(HC03)2 + Ca(OH)2 \( \to \) 2CaC03\( \downarrow \) + 2H20
Ca2+ + HC\({O_3}^ - \) + O\({H^ - }\) \( \to \) CaC03\( \downarrow \) + H20
Mg(HC03)2 + 2Ca(OH)2 \( \to \) Mg(OH)2\( \downarrow \) + 2CaC03\( \downarrow \) + 2H20
Mg2+ + 2HC\({O_3}^ - \) + 2Ca2+ + 4O\({H^ - }\) \( \to \) Mg(OH)2\( \downarrow \) + 2CaC03\( \downarrow \) + 2H20
MgCl2 + Ca(OH)2 \( \to \) Mg(OH)2\( \downarrow \) + CaCl2
Mg2+ + 2O\({H^ - }\) \( \to \) Mg(OH)2\( \downarrow \)
CaCl2 + Na2C03 \( \to \) CaC03\( \downarrow \) + 2NaCl
Ca2+ + \(C{O_3}^{2 - }\) \( \to \) CaC03\( \downarrow \)
Bài tập 1.47 trang 10 sách bài tập(SBT) hóa học 11
Có 6 dung dịch đựng trong 6 lọ mất nhãn : Mg(N03)2, Zn(N03)2, Pb(N03)2, AlCl3, KOH và NaCl. Chỉ dùng thêm dung dịch AgN03 và một thuốc thử nữa, hãy trình bày cách nhận biết từng dung dịch. Viết các phương trình hoá học dưới dạng phân tử và ion rút gọn của các phản ứng nhận biết đó.
Hướng dẫn giải
Dùng dung dịch phenolphtalein nhận ra dung dịch KOH.
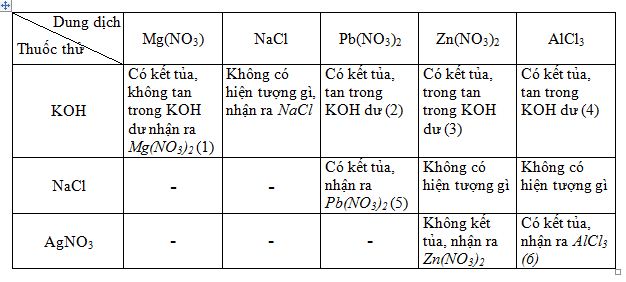
Các phương trình hoá học :
(1) Mg(N03)2 + 2KOH \( \to \) \(Mg{(OH)_2} \downarrow + 2KN{O_3}\)
Mg2+ + 2\(O{H^ - }\) \( \to \) \(Mg{(OH)_2} \downarrow \)
(2) Pb(N03)2 + 2KOH \( \to \) \(Pb{(OH)_2} \downarrow + 2KN{O_3}\)
Pb2+ + 2\(O{H^ - }\) \( \to \) \(Pb{(OH)_2} \downarrow \)
Pb(OH)2 + 2KOH \( \to \) \({K_2}Pb{O_2} + 2{H_2}O\)
Pb(OH)2 + 2\(O{H^ - }\) \( \to \) \(Pb{O_2}^{2 - } + 2{H_2}O\)
(3) Zn(N03)2 + 2KOH \( \to \) \(Zn{(OH)_2} \downarrow + 2KN{O_3}\)
Zn2+ + 2\(O{H^ - }\) \( \to \) \(Zn{(OH)_2} \downarrow \)
Zn(OH)2 + 2KOH \( \to \) \({K_2}Zn{O_2} + 2{H_2}O\)
Zn(OH)2 + 2\(O{H^ - }\) \( \to \) \(Zn{O_2}^{2 - } + 2{H_2}O\)
(4) AlCl3 + 3KOH \( \to \) \(Al{(OH)_3} \downarrow + 3KCl\)
Al3+ + 3\(O{H^ - }\) \( \to \) \(Al{(OH)_3} \downarrow \)
Al(OH)3 + KOH \( \to \) \(KAl{O_2} + 2{H_2}O\)
Al(OH)3 + \(O{H^ - }\) \( \to \) \(Al{O_2}^ - + 2{H_2}O\)
(5) 2NaCl + Pb(N03)2 \( \to \) \(2NaN{O_3} + PbC{l_2} \downarrow \)
Pb2+ + 2\(C{l^ - }\) \( \to \) \(PbC{l_2} \downarrow \)
(6) 3AgN03 + AlCl3 \( \to \) \(Al{(N{O_3})_3} + 3AgCl \downarrow \)
Ag+ + \(C{l^ - }\) \( \to \) \(AgCl \downarrow \)




