Bài 39: Dẫn xuất halogen của hiđrocacbon
Bài tập trắc nghiệm 8.1, 8.2, 8.3 trang 57 sách bài tập(SBT) hóa học 11
8.1. Chất nào sau đây là dẫn xuất halogen của hiđrocacbon ?
A. Cl-CH2-COOH
B. C6H5-CH2-Cl
C. CH3-CH2-Mg-Br
D. CH3-CO-Cl
8.2. Chất nào sau đây không phải là dẫn xuất halogen của hiđrocacbon ?
A. CH2=CH-CH2Br
B. ClBrCH-CF3
C. Cl2CH-CF2-O-CH3
D. C6H6Cl6
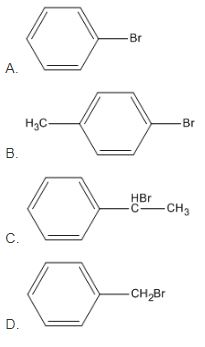
8.3. Benzyl bromua có công thức cấu tạo nào trong số các công thức dưới đây ?
Hướng dẫn giải
8.1. B
8.2. C
8.3. D
Bài tập 8.4 trang 57 sách bài tập(SBT) hóa học 11
Viết phương trình hoá học thực hiện các biến hoá dưới đây, nêu rõ điều kiện của phản ứng và ghi tên các chất.
\(C{H_4}\) ![]() ?
? ![]() \({C_2}{H_4}\)
\({C_2}{H_4}\) ![]() ?
?![]() \(C{H_2} = CH - Cl\)
\(C{H_2} = CH - Cl\) ![]() PVC
PVC
Hướng dẫn giải
(1) 2\(C{H_4}\) ![]() + 3\({H_2}\)
+ 3\({H_2}\)
metan axetilen
(2) ![]() + \({H_2}\)
+ \({H_2}\) ![]() \(C{H_2} = C{H_2}\)
\(C{H_2} = C{H_2}\)
eten
(3) \(C{H_2} = C{H_2}\) + \(C{l_2}\) \( \to \) \(Cl - C{H_2} - C{H_2} - Cl\)
1,2-đicloetan
(4) \(Cl - C{H_2} - C{H_2} - Cl\) + KOH ![]() \(C{H_2} = C{H_2} - Cl + KCl + {H_2}O\)
\(C{H_2} = C{H_2} - Cl + KCl + {H_2}O\)
vinyl clorua
(5) \(C{H_2} = C{H_2} - Cl\) .bmp)
Bài tập 8.5 trang 57 sách bài tập(SBT) hóa học 11
Viết phương trình hoá học của các phản ứng thực hiện các biến hoá dưới đây :
.bmp)
Ở đây A và B là các sản phẩm chính của phản ứng. Hãy viết các chất hữu cơ dưới dạng công thức cấu tạo
Hướng dẫn giải
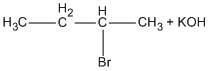
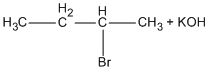
![]() \(C{H_3} - CH = CH - C{H_3} + KBr + {H_2}O\)
\(C{H_3} - CH = CH - C{H_3} + KBr + {H_2}O\)
.bmp)
![]()
Bài tập 8.6 trang 58 sách bài tập(SBT) hóa học 11
Đốt cháy hoàn toàn 3,96 g chất hữu cơ A, thu được 1,792 lít C02 (đktc) và 1,440 g H20. Nếu chuyển hết lượng clo có trong 2,475 g chất A thành AgCl thì thu được 7,175 g AgCl.
1. Xác định công thức đơn giản nhất của A.
2. Xác định công thức phân tử của A biết rằng tỉ khối hơi của A đối với etan là 3,3.
3. Viết các công thức cấu tạo mà A có thể có và ghi tên từng chất theo hai cách đọc tên khác nhau.
Hướng dẫn giải
1. Khi đốt cháy A ta thu được C02 và H20; vậy A phải chứa C và H.
Khối lượng C trong 1,792 lít C02 là : \(\frac{{12.1,792}}{{22,4}}\) = 0,96 (g).
Khối lượng H trong 1,44 g H20 : \(\frac{{2.1,44}}{{18}}\) = 0,16 (g).
Đó cũng là khối lượng C và H trong 3,96 g A.
Theo đầu bài A phải chứa Cl. Khối lượng Cl trong 7,175 g AgCl :
\(\frac{{35,5.7,175}}{{143,5}} = 1,775(g)\)
Đó cũng là khối lượng Cl trong 2,475 g A.
Vậy, khối lượng Cl trong 3,96 g A : \(\frac{{1,775.3,96}}{{2,475}}\) = 2,840 (g).
Khối lượng C, H và Cl đúng bằng khối lượng chất A (3,96 g).
Vậy, chất A có dạng CxHyClz.
x : y : z = \(\frac{{0,96}}{{12}}:\frac{{0,16}}{1}:\frac{{2,84}}{{35,5}}\) = 0,08 : 0,16 : 0,08 = 1 : 2 : 1
CTĐGN của A là CH2Cl.
2. MA = 3,3.30 = 99 (g/mol)
\( \Rightarrow {(C{H_2}Cl)_n}\) = 99 \( \Rightarrow \) 49,5n = 99 \( \Rightarrow \) n = 2
CTPT của A là C2H4Cl2.
3. Các CTCT
.bmp) 1,1-đicloetan
1,1-đicloetan
.bmp) 1,2-đicloetan (etylen clorua)
1,2-đicloetan (etylen clorua)




