Bài 3: Sự điện li của H2O - pH - Chất chỉ thị axit-bazo
Bài 2 (SGK trang 14)
Phát biểu các định nghĩa môi trường axit, trung tính, và kiềm theo nồng độ H+ và pH.
Hướng dẫn giải

Bài 3 (SGK trang 14)
Chất chỉ thị axit-bazo là gì? Hãy cho biết màu của quỳ và phenolphtalen trong dinh dịch với các khoảng pH khác nhau?
Hướng dẫn giải
Để xác định môi trường của dung dịch người ta thường dùng chất chỉ thị axit-bazo. Chất chỉ thị axit-bazo là chất có màu biến đổi phụ thuộc vào pH của dung dịch.
Màu của quỳ tím và phenolphtalen trong dung dịch có khoảng pH khác nhau:

Bài 1 (SGK trang 14)
Tích số ion của nước là gì và bằng bao nhiêu ở 25 độ C?
Hướng dẫn giải
Tích nồng độ ion H+ và nồng độ ion OH^– trong nước gọi là tích số ion của nước. Ở 25°c, tích số này có giá trị 10^-14
Bài 4 (SGK trang 14)
Một dung dịch có [OH-] = 1,5.10-5 M. Môi trường của dung dịch này là
A. axit
B. trung tính
C. kiềm
D. không xác định được
Hướng dẫn giải
Đáp án C
Một dung dịch có [OH- ]= 1,5.10-5M.
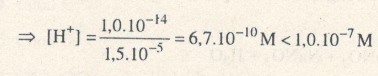
Vậy dung dịch có môi trường kiềm.
Bài 5 (SGK trang 14)
Tính nồng độ H+, OH- và pH dung dịch HCl 0,10M và dung dịch NaOH 0,010M
Hướng dẫn giải
HCl —> H+ + Cl-
0,10M 0,10M
Dung dịch HCl 0,10M có:
[H+] = 0,1M
pH = -log [H+] = 1,0
[OH-] = 1,0.10-13/[H+] = 1,0.10-13M
NaOH —> Na+ + OH-
0,010M 0,010M
Dung dịch NaOH 0,010M có:
[OH-] = 0,01M
[H+] = 1,0.10-13/[OH-] = 10-12M
pH = -log [H+] =12
Bài 6 (SGK trang 14)
Trong dung dịch HCl 0,010M, tích số ion của nước là
A. [H+].[OH-] > 1,0.10-14
B. [H+].[OH-] = 1,0.10-14
C. [H+].[OH-] < 1,0.10-14
D. không xác định được.
Hướng dẫn giải
Đáp án B




