Phương pháp giải
Một số dạng bài thường gặp:
+ Bài toán liên quan đến đồng vị
+ Xác định các nguyên tố trong cùng chu kì hoặc cùng phân nhóm
+ Bài toán hỗn hợp kim loại
Ví dụ minh họa
Ví dụ 1: Cho m gam hỗn hợp bột X gồm 3 kim loại Zn, Cr, Sn có số mol bằng nhau tác dụng hết với lượng dư dung dịch HCl loãng, nóng thu được dung dịch Y và khí H2. Cô cạn dung dịch Y thu được 8,98 g muối khan. Nếu cho m gam hỗn hợp X tác dụng vói O2 lấy dư để tạo hỗn hợp 3 oxit thì thể tích khí O2 phản ứng là
A. 2,016 lít.
B. 0,672 lít.
C. 1,344 lít.
D. 1,008 lít.
Giải
Ba kim loại Zn, Cr, Sn khi tác dụng với HCl loãng nóng đều bị oxi hóa lên số oxi hóa +2. Gọi X là kim loại chung thỏa mãn tính chất khi tác dụng với HCl giống với 3 kim loại trên.
3 kim loại có số mol bằng nhau
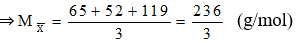

Muối khan khi cô cạn dung dịch Y là hỗn hợp muối clorua của 3 kim loại (XCl2 )

Ba kim loại có số mol bằng nhau

Phản ứng với Oxi

⇒Đáp án D
Ví dụ 2: X và Y là hai nguyên tố halogen ở 2 chu kì liên tiếp trong bảng tuần hoàn. Để kết tủa hết ion trong dung dịch chứa 4,4 gam muối natri của chúng cần 150 ml dung dịch AgNO3 0,4 M. X và Y là
A. Flo, clo.
B. Clo, brom.
C. Brom, iot.
D. Không xác định.
Giải:
Ta có nAgNO3= 0,06 mol.
Gọi công thức trung bình của 2 muối là NaR

Mà 2 halogen thuộc chu kỳ liên tiếp
Nên 2 halogen đó là Cl (35,5) và Br (80).
⇒Đáp án B
Ví dụ 3: Cho dung dịch chứa 6,03 gam hỗn hợp gồm hai muối NaX và NaY (X, Y là hai nguyên tố có trong tự nhiên, ở hai chu kì liên tiếp thuộc nhóm VIIA, số hiệu nguyên tử ZX < ZY) vào dung dịch AgNO3 (dư), thu được 8,61 gam kết tủa. Thành phần phần trăm khối lượng của NaX trong hỗn hợp ban đầu là
A. 47,2 %
B. 52,8%
C. 58,2%
D. 41,2%
Giải:
Gỉa sử Y không phải Flo

⇒X là Clo, Y là Flo
Kết tủa chỉ gồm AgCl; nAgCl = nNaCl = 8,61 : 143,5 = 0,06 mol
% mNaCl = 0,06.58,5 : 6,03 . 100% = 58,2% => % mNaF = 41,2%
⇒Đáp án D
Ví dụ 4: Cho 1,9 gam hỗn hợp muối cacbonat và hiđrocacbonat của kim loại kiềm M tác dụng hết với dung dịch HCl (dư), sinh ra 0,448 lít khí (ở đktc). Kim loại M là:
A. K
B. Rb
C. Na
D. Li
Giải:
Công thức muối cacbonat và hiđrocacbonat của kim loại kiềm M là M2CO3 và MHCO3.
Phương trình phản ứng hóa học :
M2CO3 + 2HCl → 2MCl + CO2 + H2O
MHCO3 + HCl → MCl + CO2 + H2O
Theo các phản ứng ta thấy: Tổng số mol hỗn hợp muối = số mol của CO2 = 0,02 mol.
Gọi khối lượng mol trung bình của hai muối là M(tb),
ta có: M + 61 < M(tb) < 2M + 60 (*)
Mặt khác M(tb) = 1,9/0,02 = 95 (**)
Kết hợp giữa (*) và (**) ⇒ 17,5 < M < 34 ⇒ Kim loại M là Na.
⇒ Đáp án C
Ví dụ 5: Nguyên tử khối trung bình của đồng kim loại là 63,546. Đồng tồn tại trong tự nhiên với hai đồng vị là

Thành phần phần trăm của đồng

theo số nguyên tử là
A. 27,30%
B. 26,30%
C. 26,7%
D. 23,70%
Giải:

Từ (1)(2) ⇒x1 = 27,3 ; x2 = 72,7
⇒ Đáp án A
Được cập nhật: 11 tháng 4 lúc 22:28:42 | Lượt xem: 411




