Kiểm tra hóa 8 chương IV: Oxi, không khí
Nội dung tài liệu
Tải xuốngCác tài liệu liên quan
-
![Đề thi học kì 1 Hóa 8 trường THCS TT Vĩnh Tường năm 2017-2018]()
-
![Đề kiểm tra học kì 1 Hóa lớp 8]()
-
![Đề thi học kì 1 Hóa lớp 8 năm 2016-2017]()
-
![Đề thi học kì 1 Hóa lớp 8]()
-
![Đề thi học kì 1 Hóa 8 trường THCS Thái Bình năm 2016-2017]()
-
![Đề thi học kì 1 Hóa 8 trường THCS Biên Giới năm 2016-2017]()
-
![Đề thi học kì 1 Hóa 8]()
-
![Đề thi học kì 1 Hóa 8 trường THCS Sơn Lâm năm 2021-2022]()
-
![Đề thi học kì 1 Hóa 8 năm 2020-2021]()
-
![Đề thi học kì 2 Hóa 8 trường PTDTBT THCS Liên xã La ÊÊ - Chơ Chun năm 2021-2022]()
Có thể bạn quan tâm
Thông tin tài liệu
KIỂM TRA 1 TIẾT HỌC KỲ II LẦN 1
MÔN HOÁ HỌC 8
I. MỤC TIÊU ĐỀ KIỂM TRA
- Đánh giá quá trình dạy và học theo mức độ đạt chuẩn kiến thức, kĩ năng trong chương oxi – không khí.
- Với mục đích đánh giá năng lực biết – hiểu và vận dụng của HS với hình thức kiểm tra trắc nghiệm và tự luận.
II. HÌNH THỨC ĐỀ KIỂM TRA
- Hình thức đề kiểm tra: trắc nghiệm và tự luận
- Cách tổ chức kiểm tra: cho học sinh làm bài kiểm tra trong 45 phút
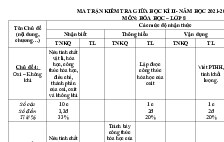
III. THIẾT LẬP MA TRẬN
- Liệt kê tất cả các chuẩn kiến thức kĩ năng của chương oxi – không khí.
- Chọn các nội dung cần đánh giá và thực hiện các bước thiết lập ma trận đề kiểm tra.
- Xác định khung ma trận.
-
Nội dung
Mức độ nhận thức
Tổng
Nhận biết
Thông hiểu
Vận dụng
Vận dụng ở mức cao hơn
TN
TL
TN
TL
TN
TL
TN
TL
Tính chất của oxi
Tính chất hóa học của oxi
4
(2,75)
27,5%
Số câu
1 (câu 13)
3 (câu 5, 9, 12)
Số điểm
2
0,75
Không khí – sự cháy
Thành phần không khí
2 (0,5)
5%
Số câu
2 (câu 2, 3)
Số điểm
0,5
Điều chế oxi
điều chế khí oxi
Tính toán
3 (5,25)
52,5%
Số câu
1 (câu 6)
2 (câu 14, 15)
Số điểm
0,25
5
Phản ứng phân hủy- phản ứng hóa hợp
2 (0,5)
Số câu
2 (câu 1,4)
5%
Số điểm
0,5
Oxit
- oxit axit
- oxit bazơ
4
(1)
Số câu
4 (câu 7, 8, 10, 11)
10%
Số điểm
1
Tổng
9
1
3
2
15
(2,25)
(2)
(0,75)
(5,0)
(10.0)
22,5%
20%
57,5%
100%
Họ và tên: ………………….................………….. KIỂM TRA 1 TIẾT LẦN 1 HKII
Lớp: 8A HÓA HỌC 8
I. TRẮC NGHIỆM: (3 điểm)
Câu 1. Trong các phản ứng sau, phản ứng nào là phản ứng hoá hợp.
A. C +
O2
C. 2Fe(OH)3
Câu 2. Trong thành phần không khí, khí oxi chiếm bao nhiêu phần trăm về thể tích:
A. 1/2 B. 2/5 C. 1/5 D. 2/4
Câu 3. Thành phần của không khí gồm:
A. 21% N2, 78% O2... B. 78% N2, 21% O2... C. 1% CO2... D. 21% O2, 1% CO2
Câu 4. Trong các phản ứng sau, phản ứng nào là phản ứng phân huỷ.
A . CaO
+ H2O
C. C +
O2
Câu 5. Thế tích khí oxi (đktc) cần dùng để đốt cháy 8,4g Fe là:
A. 22,4(l) B. 2,24 (l) C. 0,224 (l) D. 11,2 (l)
Câu 6. Trong các chất sau, chất nào được dùng để điều chế khí oxi trong phòng thí nghiệm.
A. CaCO3 B. Fe2O3 C. H2O D. KMnO4
Câu 7. Dãy oxit nào sau đây là oxit bazơ:
a) SO3, CaO, MgO b) CaO, MgO, K2O
c) SO3, P2O5, CuO d) CuO, CO2, CaO
Câu 8. Oxit Al2O3 có bazơ tương ứng là:
a) Al(OH)2 b) Al(OH)3 c) Al3(OH) d) AlOH3
Câu 9. Khử 40g sắt (III) oxit thu được 14g sắt. Thể tích khí CO cần dùng là:
a) 8,4 lít b) 8,6 lít c) 9,2 lít d) 11,2 lít
Câu 10. Hợp chất nào sau đây thuộc loại oxit axit:
a) CuO b) Fe2O3 c SO2 d) Na2O
Câu 11. Oxit CO2 có axit tương ứng là:
A. HCO2 B. H2CO3
C. CO3 D. CaCO3
Câu 12. Thể tích của 3,2gam khí SO2 (đktc) là:
A.1,12 lít B.1,2 lít C.2,24 lít D.1,1 lít.
II. TỰ LUẬN: (7điểm)
Câu 13. Hoàn thành các phương trình hóa học sau: (2 điểm)
a)
b)
c)
d)
Câu 14. Nung nóng kali clorat KClO3 thu được 3,36 lít khí oxi (đktc) (2,5 điểm)
a) Viết phương trình phản ứng
b) Tính khối lượng KClO3 cần dùng.
Câu 15. Đem phân huỷ hoàn toàn 15,8 gam KMnO4. (2,5 điểm)
a) Viết phương trình hóa học.
b) Tính thể tích khí oxi thu được ở điều kiện tiêu chuẩn.
Biết: Fe = 56 ; O =16 ; Mn = 55 ; K = 39 ; Cl = 35,5
ĐÁP ÁN ĐỀ KIỂM TRA HÓA 8 CHƯƠNG OXI-KHÔNG KHÍ
1. TRẮC NGHIỆM (3 điểm)
Câu |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
Đáp án |
A |
C |
B |
C |
B |
D |
B |
B |
A |
C |
B |
A |
mỗi câu đúng 0,25 điểm
II.TỰ LUẬN (7 điểm)
Câu 13.
a)
b)
c)
d)
mỗi câu đúng 0,5 điểm, nếu không đúng không cho điểm, nếu không ghi điều kiện phản ứng vẫn cho điểm tối đa.
Câu 14.
a) Viết phương trình phản ứng
- Tìm số mol khí oxi:
b)
2mol 3mol
xmol 0,15mol
→ x = 0,1(mol)
Tính khối lượng KClO3 cần dùng: m = n.M = 0,1(mol).122,5(g/mol)=12,25(g) 0,75 điểm
Câu 15.
Đem phân huỷ hoàn toàn 15,8 gam KMnO4. (2,5 điểm)
a) Viết phương trình hóa học.
b) Tính thể tích khí oxi thu được ở điều kiện tiêu chuẩn.
- Tìm số mol KMnO4:
b)
2mol 1mol
0,1mol xmol
→ x = 0,05(mol)
Tính thể tích khí oxi thu được (ở đktc): V = n.22,4 = 0,05(mol).22,4(g/mol)=1,12(l)
0,75 điểm
Số điểm |
0 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
|
|
|
|
|
|
|
|
|
|
|