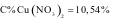Đề thi giữa kì 1 Hóa 11 trường THPT Cầm Xuyên
Nội dung tài liệu
Tải xuốngCác tài liệu liên quan
-
![Đề thi học kì 2 Hóa 11 năm 2016-2017]()
-
![Đề thi học kì 2 Hóa 11 năm 2020-2021 ĐỀ 1]()
-
![Đề thi học kì 2 Hóa 11 năm 2020-2021 ĐỀ 4]()
-
![Đề thi học kì 2 Hóa 11 năm 2020-2021 ĐỀ 7]()
-
![Đề thi học kì 2 Hóa 11 năm 2020-2021 ĐỀ 2]()
-
![Đề thi học kì 2 Hóa 11 năm 2020-2021 ĐỀ 5]()
-
![Đề thi học kì 2 Hóa 11 năm 2020-2021 ĐỀ 6]()
-
![Đề thi học kì 2 Hóa 11 năm 2020-2021 ĐỀ 3]()
-
![Đề thi học kì 2 Hóa 11 trường THPT Thống Nhất mã đề 01 năm 2020-2021]()
-
![Đề thi học kì 2 Hóa 11 trường THPT Thống Nhất mã đề 02 năm 2020-2021]()
Có thể bạn quan tâm
Thông tin tài liệu
TRƯỜNG THPT CẨM XUYÊN ĐỀ THI GIỮA KÌ I HÓA 11 Đề 01
NHÓM: HÓA
Họ và tên học sinh: …………………………………………..
I/ Phần 1: trắc nghiệm: (7đ)
Câu 1: Chất nào sau đây,khi tan trong nước là chất điện li mạnh:
A. Fe(OH)3. B. CH3COOH. C. Ba(OH)2. D. H2S
Câu 2: Chất nào sau đây là hidroxit lưỡng tính:
A. Fe(OH)3 B. Al(OH)3 C. Mg(OH)2 D. Fe(OH)2
Câu 3: Cho các dung dịch có cùng nồng độ. Dung dịch nào sau đây dẫn điện kém nhất
A. H2S B. HCl C. FeCl2. D. Ca(OH)2
Câu 4:Theo thuyết Arehinut, chất nào sau đây là axit?
A. KOH B. H2SO4 C. CuCl2 D. NH4Cl
Câu 5: Cho phản ứng Al + HNO3 --> Al(NO3)3 + N2O + H2O. Tổng hệ số tối giản cảu phương trình sau khi cân bằng là:
A. 66 B. 64 C. 68 D. 77
Câu 6: Cho các dung dịch riêng biệt có cùng nồng độ 1M . Dung dịch có pH bé nhất là:
A. HNO3 B. NaCl C. H2SO4 D. NaOH
Câu 7: Cho dung dịch BaCl2 vào dung dịch nào sau đây thu được kết tủa?
A. Na2CO3. B. NaHCO3 C. Ca(NO3)2 D. MgCl2
Câu 8: Nhiệt phân hoàn toàn Cu(NO3)2 thu được sản phẩm là:
A. CuO, NO2, O2 B. Cu, NO2, O2 C. Cu(NO3)2, CuO, NO2, O2 D. O2, Cu(NO2)2
Câu 9: Dung dịch HNO3 đậm đặc trong phòng thí nghiệm có màu:
A. Không màu B. nâu C. Đỏ sẩm D. vàng
Câu 10: Dung dịch có pH = 7 là:
A.Na2CO3 B. NH4HSO4 C. CH3COONa D. CaCl2
Câu 11: Cho dung dịch Ca(HCO3)2 tác dụng với chất nào sau đây sinh ra kết tủa:
A. NaCl. B. KOH. C.NaHCO3. D. HCl
Câu 12: Dung dịch chất nào sau đây làm quỳ tím hóa xanh:
A. NH3 B. HCl C. KCl D. HF
Câu 13: Kim loại không tác dụng với dung dịch HNO3 đặc, nguội là:
A. Mg B. Cu C. Ag D. Fe
Câu 14: Chất được dùng làm bột nở là:
A. Na2CO3 B. NaHCO3 C. CaCO3 D. NaOH
Câu 15: Cho Al vào dung dịch HNO3 vừa đủ thu được dung dịch X mà không có khí thoát ra, các chất tan trong X là:
A. Al(NO3)2 B. Al(NO3)3 C. NH4NHO3 D. NH4NO3, Al(NO3)3
Câu 16: Cho 300 ml dung dịch KOH 1M vào 400 ml dung dịch FeCl3 1M thu được số gam kết tủa là:
A. 10,7 B. 32,1 C. 21,4 D. 42,8
Câu 17: Cho m gam hỗn hợp X gồm CuO, ZnO, MgO, Al2O3 tác dụng vừa đủ với 500ml dung dịch HCl 1M thu được dung dịch X. Cô cạn dung dịch X thu được 36,5 gam chất rắn khan. Giá trị của m là:
A. 25,75 . B. 18,75 . C. 22,75. D. 17,75.
Câu 18: Cho 14 gam Fe vào dung dịch HNO3 dư thu được dung dịch X và V lít khí NO đktc ( sản phẩm khử duy nhất). Giá trị của V là:
A. 4,48 B. 6,72 C. 3,36 D. 5,6
Câu 19: Một dung dịch có chứa 2 cation là
Mg2+ (x mol); Fe3+ (y mol) và 2 anion là
Cl- (0,4 mol);  (0,3
mol). Khi cô cạn dung dịch thu được 59 gam muối khan. Giá trị của x và y
lần lượt là:
(0,3
mol). Khi cô cạn dung dịch thu được 59 gam muối khan. Giá trị của x và y
lần lượt là:
A. 0,3 và 0,2. B. 0,4 và 0,45. C. 0,2 và 0,2. D. 0,5 và 0,4.
Câu 20: Cho 300 ml dung dịch H3PO4 1M vào 300 ml dung dịch NaOH 2M thu được dung dịch chứa muối là:
A. NaH2PO4 B. Na2HPO4 C. Na3PO4 D. Cả A và B
Câu 21: Trộn 100 ml dung dịch gồm Ba(OH)2 0,1M và NaOH 0,2M với 400 ml dung dịch gồm H2SO4 0,03125M và HCl 0,025M thu được dung dịch X.Giá trị pH của dung dịch X là:
A. 1. B. 2 C. 12 D. 13
Câu 22: Dung dịch E chứa các ion Fe3+, SO42-, NH4+, HCO3-. Chia dung dịch E ra 2 phần bằng nhau:
+ Phần I tác dụng với dung dịch NaOH dư, đun nóng, được 16,05 gam kết tủa và 8,96 lit khí (đktc).
+ Phần II tác dụng với dung dịch BaCl2 dư, được 46,6 gam kết tủa.
Cô cạn E thu được số gam chất rắn khan là:
A. 60. B. 96,6. C. 124,5. D. 48,3.
Câu 23: Cho các mệnh đề sau:
1. Phương trình ion thu gọn cho biết bản chất của phản ứng trao đổi trong dung dịch chất điện li.
2. Axit mạnh là chất điện li mạnh.
3. Nhiệt phân NH4Cl là phản ứng oxi hóa khử.
4. Amoniac lỏng được dùng làm chất làm lạnh trong các thiết bị lạnh.
5. KNO3 được dùng để chế thuốc nổ không khói.
6. NH4HCO3 dùng làm xốp bánh.
7. HNO3 là được dùng để sản xuất thuốc nổ, thuốc nhuộm, dược phẩm
8. H3PO4 là axit 3 nấc có độ mạnh trung bình, tác dụng được với dung dịch kiềm.
Số mệnh đề đúng là:
A. 5 B. 6 C. 7. D. 8
Phần II/ Tự luận.(3đ)
Câu 1: Viết PT ion rút gọn xảy ra ( nếu có)
a. HNO3 + NaOH b. Na2SO4 + BaCl2
d. MgCO3 + HNO3 e. Ba(HCO3)2 + NaOH
Câu 2. Hòa tan 17,32 gam hỗn hợp X gồm Mg, Fe3O4 và Fe(NO3)2 cần vừa đúng dung dịch hỗn hợp gồm 1,04 mol HCl và 0,08 mol HNO3, đun nhẹ thu được dung dịch Y và 2,24 lít hỗn hợp khí Z (đktc) có tỉ khối hơi đối với H2 là 10,8 gồm hai khí không màu trong đó có một khí hóa nâu ngoài không khí. Cho dung dịch Y tác dụng với một lượng dung dịch AgNO3 vừa đủ thu được m gam kết tủa và dung dịch T. Cho dung dịch T tác dụng với một lượng dư dung dịch NaOH, lọc kết tủa nung đến đến khối lượng không đổi thu được 20,8 gam chất rắn. Các phản ứng xảy ra hoàn toàn. Tính m?
(Cho H=1, O=16,Fe=56, N=14, S=32, Cl=35,5, Mg=24, Al=27, C=12, Ba=137, Ca=40, P=31, Zn=65, Ag=108, Ba=137)
Đáp án A








TRƯỜNG THPT CẨM XUYÊN ĐỀ THI GIỮA KÌ I HÓA 11 Đề 01
NHÓM: HÓA
Họ và tên học sinh: …………………………………………..
I/ Phần 1: trắc nghiệm: (7đ)
Câu 1: Chất nào sau đây,khi tan trong nước là chất điện li yếu:
A. NaCl. B. HNO3. C. Ba(OH)2. D. H2S
Câu 2: Chất nào sau đây là hidroxit lưỡng tính:
A. Fe(OH)3 B. Mg(OH)2 C. Zn(OH)2 D. Fe(OH)2
Câu 3: Cho các dung dịch có cùng nồng độ. Dung dịch nào sau đây dẫn điện tốt nhất
A. H2S B. HCl C. NaOH. D. Ca(OH)2
Câu 4:Theo thuyết Arehinut, chất nào sau đây là axit?
A. KOH B. H2SO4 C. CuCl2 D. NH4Cl
Câu 5: Cho phản ứng Mg + HNO3 --> Mg(NO3)2 + N2 + H2O. Tổng hệ số tối giản cảu phương trình sau khi cân bằng là:
A. 29 B. 28 C. 30 D. 32
Câu 6: Cho các dung dịch riêng biệt có cùng nồng độ 1M . Dung dịch có pH lớn nhất là:
A. HNO3 B. Ca(OH)2 C. H2SO4 D. NaOH
Câu 7: Cho dung dịch AgNO3 vào dung dịch nào sau đây thu được kết tủa?
A. NaNO3. B. NaHCO3 C. Ca(NO3)2 D. MgCl2
Câu 8: Nhiệt phân hoàn toàn AgNO3 thu được sản phẩm là:
A. Ag2O, NO2, O2 B. Ag, NO2, O2 C. AgNO3,, NO2, O2 D. O2, AgNO2
Câu 9: Người ta dùng bình thủy tinh đựng dung dịch HNO3 đậm đặc có màu:
A. Không màu B. Sáng trắng C. Tối màu D. vàng
Câu 10: Dung dịch có pH > 7 là:
A.HCl B. NH4HSO4 C. CH3COONa D. CaCl2
Câu 11: Cho dung dịch Ba(HCO3)2 tác dụng với chất nào sau đây sinh ra kết tủa:
A. NaCl. B. KNO3. C.NaHCO3. D. KOH
Câu 12: Dung dịch chất nào sau đây làm quỳ tím hóa đỏ:
A. NH3 B. HNO3 C. KCl D. NaOH
Câu 13: Kim loại không tác dụng với dung dịch HNO3 đặc, nguội là:
A. Al B. Cu C. Ag D. Na
Câu 14: Chất được dùng làm thuốc chữa đau dạ dày là:
A. Na2CO3 B. NaHCO3 C. CaCO3 D. NaOH
Câu 15: Cho Mg vào dung dịch HNO3 vừa đủ thu được dung dịch X mà không có khí thoát ra, các chất tan trong X là:
A. Mg(NO3)2 B. MgNO3)3 C. NH4NO3, Mg(NO3)2 D. NH4NO3
Câu 16: Cho 300 ml dung dịch KOH 1M vào 400 ml dung dịch FeCl2 1M thu được số gam kết tủa là:
A. 10,7 B. 13,5 C. 27 D. 36
Câu 17: Cho 32,5 gam hỗn hợp X gồm CuO, ZnO, MgO, Al2O3 tác dụng vừa đủ với 600ml dung dịch HCl 1M thu được dung dịch X. Cô cạn dung dịch X thu được m gam chất rắn khan. Giá trị của m là:
A. 49 . B. 53,8 . C. 58,3 D. 54,4
Câu 18: Cho m gam Mg vào dung dịch HNO3 dư thu được dung dịch X và 6,72 lít khí NO đktc ( sản phẩm khử duy nhất). Giá trị của m là:
A. 5,4 B. 21,6 C. 10,8 D. 26,1
Câu 19: Một dung dịch có chứa 2 cation là
Zn2+ (x mol); Fe3+ (y mol) và 2 anion là
Cl- (0,4 mol);  (0,2
mol). Khi cô cạn dung dịch thu được 51,1 gam muối khan. Giá trị của x và
y lần lượt là:
(0,2
mol). Khi cô cạn dung dịch thu được 51,1 gam muối khan. Giá trị của x và
y lần lượt là:
A. 0,1 và 0,2. B. 0,2 và 0,25. C. 0,2 và 0,2. D. 0,2 và 0,3.
Câu 20: Cho 200 ml dung dịch H3PO4 1M vào 300 ml dung dịch NaOH 2M thu được dung dịch chứa muối là:
A. NaH2PO4 B. Na2HPO4 C. Na3PO4 D. Cả A và B
Câu 21: Trộn 100 ml dung dịch gồm Ba(OH)2 0,1M và NaOH 0,2M với 400 ml dung dịch gồm H2SO4 0,04375M và HCl 0,025M thu được dung dịch X.Giá trị pH của dung dịch X là:
A. 1. B. 2 C. 12 D. 13
Câu 22: Dung dịch E chứa các ion Fe2+, SO42-, NH4+, HCO3-. Chia dung dịch E ra 2 phần bằng nhau:
+ Phần I tác dụng với dung dịch NaOH dư, đun nóng, được 9 gam kết tủa và 4,48 lit khí (đktc).
+ Phần II tác dụng với dung dịch BaCl2 dư, được 23,3 gam kết tủa.
Cô cạn E thu được số gam chất rắn khan là:
A. 62. B. 31. C. 49,6. D. 24,8.
Câu 23: Cho các mệnh đề sau:
1. Phương trình ion thu gọn cho biết bản chất của phản ứng trao đổi trong dung dịch chất điện li.
2. Bazo mạnh là chất điện li mạnh.
3. Nhiệt phân NH4HCO3 là phản ứng oxi hóa khử.
4. Nito lỏng được dùng để bảo quản máu và các mẫu vật.
5. KNO3 được dùng để chế thuốc nổ có khói.
6. NH4HCO3 dùng làm xốp bánh.
7. HNO3 là được dùng để sản xuất thuốc nổ, thuốc nhuộm, dược phẩm
8. H3PO4 là axit 3 nấc có độ mạnh trung bình, tác dụng được với dung dịch kiềm.
Số mệnh đề đúng là:
A. 5 B. 6 C. 7. D. 8
Phần II/ Tự luận.(3đ)
Câu 1: Viết PT ion rút gọn xảy ra ( nếu có)
a. HNO3 + KOH b. Na2CO3 + Ba(NO3)2
d. CaCO3 + HNO3 e. Ca(HCO3)2 + KOH
Câu 2. Hòa tan hoàn toàn 11,6 gam hỗn hợp A gồm Fe và Cu vào 87,5 gam dung dịch HNO3 50,4%, sau khi kim loại tan hết thu được dung dịch X. Cho 500ml dung dịch KOH 1M vào dung dịch X thu được kết tủa Y và dung dịch Z. Lọc lấy Y rồi nung trong không khí đến khối lượng không đổi thu được 16 gam chất rắn. Cô cạn dung dịch Z được chất rắn T. Nung T đến khối lượng không đổi thu được 41,05 gam chất rắn. Nồng độ phần trăm của muối Fe(NO3)3 có trong dung dịch X gần nhất với giá trị nào sau đây?
(Cho H=1, O=16,Fe=56, N=14, S=32, Cl=35,5, Mg=24, Al=27, C=12, Ba=137, Ca=40, P=31, Zn=65, Ag=108, Ba=137)
Câu 77: Chọn B.
>> Lập hệ khối lượng kim loại (11,6 gam) và khối lượng 2 oxit kim loại (16 gam) tính được:

>> Lập hệ tổng khối lượng chất rắn (KNO2 & KOH dư) 41,05 gam và tổng số mol (0,5 mol, bằng KOH ban đầu) tính được:
 dư = 0,05
dư = 0,05

Bảo toàn  thoát ra ở khí
thoát ra ở khí 
Nhận thấy  Tạo ra cả muối Fe3+ (a) và
Tạo ra cả muối Fe3+ (a) và 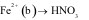 đã hết.
đã hết.


 và b = 0,1
và b = 0,1
Phần khí quy đổi thành N (0,25) và O (u mol)
Bảo toàn electron:

 m kim loại +
m kim loại + 
Dung dịch Z chứa 3 muối  và
và  và
và 

C%Fe(NO3)2 = 20,18%