Lý thuyết và Phương pháp giải
CTTQ este: CnH2n+2-2k-2xO2x
PT tổng quát
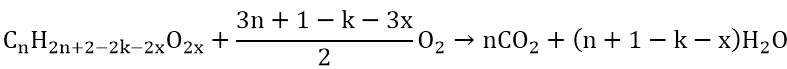
TH este no, đơn chức

⇒ nH2O = nCO2 ; neste = 1,5nCO2 - nO2
⇒ Số nguyên tử C là

Trường hợp đốt cháy một hỗn hợp nhiều este thuộc cùng dãy đồng đẳng thì ta cũng kết luận tương tự như trên.
nhỗn hợp = 1,5nCO2 - nO2

ở đây :

,với nmin < n– < nmax
khác với axit cacboxylic giá trị n– trong este luôn lớn hơn 2.
Ví dụ minh họa
Bài 1: Đốt cháy hoàn toàn 7,4 gam este X đơn chức thu được 6,72 lít khí CO2 (đktc) và 5,4 gam nước. Xác định công thức phân tử của X.
Hướng dẫn:
Ta có : nCO2 = 6,72/22,4 = 0,3 (mol) và nH2O = 5,4/18 = 0,3 (mol)
Vì khi đốt cháy X thu được nH2O = nCO2 nên X là este no đơn chức
Gọi công thức của este no, đơn chức là : CnH2nO2 (n ≥ 2)

Theo đề bài, ta có: MX = (0,3/n).(14n + 32) = 7,4 ⇒ n = 3
Vậy công thức phân tử của X là : C3H6O2.
Bài 2: Đốt cháy hoàn toàn 1,76 gam một este X thu được 3,52 gam CO2 và 1,44 gam H2O. Xác định công thức phân tử của X?
Hướng dẫn:
Ta có: nCO2 = 3,52/44 = 0,08 (mol); nH2O = 1,44/18 = 0,08(mol)
Do nCO2 = nH2O ⇒ X có độ bất bão hòa của phân tử ∆ = 1
X là este no, đơn chức ⇒ X dạng CnH2nO2

Vậy công thức phân tử của X là : C4H8O2
Bài 3: Đốt cháy hoàn toàn 4,2 gam một este E thu được 6,16 gam CO2 và 2,52 gam H2O. Xác định công thức phân tử , công thức cấu tạo , gọi tên E.
Hướng dẫn:
Ta có; nCO2 = 6,16/44 = 0,14(mol); nH2O = 2,52/18 = 0,14 (mol)
Do nCO2 = nH2O ⇒ ∆ = 1 ⇒ E là este no,đơn chức dạng: CnH2nO2

n = 2 ⇒ C2H4O2 ⇒ CTPT của E là HCOOCH3 (metyl fomiat)
Bài 4: Đốt cháy hoàn toàn một lượng hỗn hợp hai este, cho sản phẩm phản ứng cháy qua bình đựng P2O5 dư, khối lượng bình tăng thêm 6,21 gam, sau đó cho qua tiếp dung dịch Ca(OH)2 dư, thu được 34,5 gam kết tủa. Các este nói trên thuộc loại gì (đơn chức hay đa chức, no hay không no)?
Hướng dẫn:
Khối lượng tăng lên của bình P2O5 là khối lượng H2 O
P2O5 + 3H2O → 2H3PO4
Có kết tủa tạo thành là do CO2 hấp thụ
CO2 + Ca(OH)2 → CaCO3 + H2O
Ta có: nCaCO3 = 34,5/100 = 0,345 (mol)
nH2O = 6,21/18 = 0,345 (mol); nCO2 = nCaCO3 = 0,345 (mol)
Số mol H2O = số mol của CO2 ⇒ ∆ = 1
Do đó, hai este đều no, đơn chức
Bài 5: Đốt cháy hoàn toàn 3,7 gam một este đơn chức X thu được 3,36 lít khí CO2 (đktc) và 2,7 gam nước. Tìm công thức phân tử của X.
Hướng dẫn:
ta có: nCO2 = 3,36/22,4 = 0,15 (mol) và nH2O = 2,7/18 = 0,15 (mol)
Vì nCO2 = nH2O ⇒ este no,đơn chức
Gọi công thức este no, đơn chức là : CnH2nO2 (n ≥ 2)

Theo đề bài, ta có phương trình:
mX = (0,15/n).(14n + 32) = 3,7 ⇒ 2,1n + 4,8 = 3,7n ⇒ n = 3
Vậy công thức phân tử của X là : C3H6O2
Được cập nhật: 17 tháng 4 lúc 2:52:02 | Lượt xem: 876




