Bài 19. Chuyển đổi giữa khối lượng, thể tích và lượng chất
Bài 19.1 Trang 27 Sách bài tập (SBT) Hóa học 8
Hãy cho biết số mol của những khối lượng chất sau :
a) 4 g cacbon ; 62 g photpho ; 42 g sắt.
b) 3,6 g nước ; 95,48 g khí cacbonic ; 14,625 g muối ăn.
Hướng dẫn giải
Số mol của những lượng chất :
a) \({n_C} = {4 \over {12}} = {1 \over 3}(mol)\) ; \({n_P} = {{62} \over {31}} = 2(mol);{n_{Fe}} = {{42} \over {56}} = 0,75(mol)\)
b) \({n_{{H_2}O}} = {{3,6} \over {18}} = 0,2(mol)\)
\({n_{C{O_2}}} = {{95,48} \over {44}} = 2,17(mol)\)
\({n_{NaCl}} = {{14,625} \over {58,5}} = 0,25(mol)\)
Bài 19.2 Trang 27 Sách bài tập (SBT) Hóa học 8
Hướng dẫn giải
Bài 19.3 Trang 27 Sách bài tập (SBT) Hóa học 8
Vẽ biểu đồ là những hình chữ nhật để so sánh thể tích những khí sau ở đktc.
a)1 g khí hiđro ; b) 24 g khí oxi ; c) 28 g khí nitơ ; d) 88 g khí cacbonic.
Hướng dẫn giải
\(\begin{gathered}
{n_{{H_2}}} = \frac{{{m_{{H_2}}}}}{{{M_{{H_2}}}}} = \frac{1}{2} = 0,5\,\,mol \hfill \\
{n_{{O_2}}} = \frac{{{m_{{O_2}}}}}{{{M_{{O_2}}}}} = \frac{{24}}{{32}} = 0,75\,\,mol \hfill \\
{n_{{N_2}}} = \frac{{{m_{{N_2}}}}}{{{M_{{N_2}}}}} = \frac{{28}}{{28}} = 1\,\,mol \hfill \\
{n_{C{O_2}}} = \frac{{{m_{C{O_2}}}}}{{{M_{C{O_2}}}}} = \frac{{88}}{{44}} = 2\,\,mol \hfill \\
\end{gathered} \)
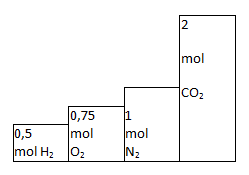
Tỉ lệ thể tích cũng chính là tỉ lệ về số mol nên ta có biểu đồ sau:
Bài 19.4 Trang 27 Sách bài tập (SBT) Hóa học 8
Hãy cho biết:
a) Số mol và số nguyên tử của : 28 g sắt (Fe) ; 6,4 g đồng (Cu) ; 9 g nhôm (Al).
b) Khối lượng và thể tích khí (đktc) của : 2 mol H2 ; 1,5 mol O2; 1,15 mol CO2 ; 1,15 mol CH4.
Hướng dẫn giải
a) 28g Fe có số mol là \({{28} \over {56}} = 0,5(mol)\) và số nguyên tử là
\(0,5 \times 6 \times {10^{23}} = 3 \times {10^{23}}\) nguyên tử (hoặc 0,5N nguyên tử).
6,4 g Cu có số mol là \({{6,4} \over {64}} = 0,1(mol)\) và số nguyên tử là
\(0,1 \times 6 \times {10^{23}} = 0,6 \times {10^{23}}\) nguyên tử ( hoặc 0,1N nguyên tử)
9g Al có số mol là \({9 \over {27}} = {1 \over 3}(mol)\) và số nguyên tử là
\((6 \times {10^{23}}):3 = 2 \times {10^{23}}\) nguyên tử ( hoặc \({N \over 3}\) nguyên tử )
b)
\({m_{{H_2}}} = 2.2 = 4g;\,\,\,{V_{{H_2}}} = 2.22,4 = 44,8\,l \\ {m_{{O_2}}} = 1,5.32 = 48g;\,\,{V_{{O_2}}} = 1,5.22,4 = 33,6\,l \\ {m_{C{O_2}}} = 1,15.44 = 50,6g;\,\,{V_{C{O_2}}} = 1,15.22,4 = 25,76\,l \\ {m_{C{H_4}}} = 1,15.16 = 18,4g;\,\,{V_{C{H_4}}} = 1,15.22,4 = 25,76\,l \)
Bài 19.5 Trang 27 Sách bài tập (SBT) Hóa học 8
Hãy tìm khối lượng của những đơn chất và hợp chất sau : CO2, H2O, N2, O2, H2, NaCl để cùng có số phân tử bằng nhau là 0,6.1023.
Hướng dẫn giải
Một mol chất (đơn chất hay hợp chất) là lượng chất có chứa 6 x 1023 phân tử (hoặc nguyên tử). Theo đề bài thì 0,6 X 1023 phân tử các chất là số phân tử có trong 0,1 mol chất. Vậy khối lượng các chất sẽ là :
- \({m_{C{O_2}}} = 0,1 \times 44 = 4,4(g)\)
- \({m_{{H_2}O}} = 0,1 \times 18 = 1,8(g)\)
- \({m_{{N_2}}} = 0,1 \times 28 = 2,8(g)\)
- \({m_{{O_2}}} = 0,1 \times 32 = 3,2(g)\)
- \({m_{{H_2}}} = 0,1 \times 2 = 0,2(g)\)
- \({m_{NaCl}} = 0,1 \times 58,5 = 5,85(g)\)
Bài 19.6 Trang 27 Sách bài tập (SBT) Hóa học 8
Phải lấy bao nhiêu gam của mỗi chất khí sau để chúng cùng có thể tích khí là 5,6 lit ở đktc ?
a)CO2 ; b) CH4 ; c) O2 ; d) N2 ; e) Cl2.
Hướng dẫn giải
Biết 5,6 lít khí ở đktc có số mol là n=\({{5,6} \over {22,4}} = 0,25(mol)\) . Để có thể tích các khí bằng nhau là 5,6 lít (đktc), ta phải lấy 0,25 mol của mỗi chất khí. Chúng có khới lượng là:
- \({m_{C{O_2}}} = 0,25 \times 44 = 11(g)\)
- \({m_{C{H_4}}} = 0,25 \times 16 = 4(g)\)
- \({m_{{O_2}}} = 0,25 \times 32 = 8(g)\)
- \({m_{{N_2}}} = 0,25 \times 28 = 7(g)\)
- \({m_{C{l_2}}} = 0,25 \times 71 = 17,75(g)\)




