Đề thi kiểm tra học kì 1 Hóa 8 trường THCS An Ngãi Trung năm 2019-2020
Nội dung tài liệu
Tải xuống
Link tài liệu:
Các tài liệu liên quan
-
![Đề thi học kì 1 Hóa 8 trường THCS TT Vĩnh Tường năm 2017-2018]()
-
![Đề kiểm tra học kì 1 Hóa lớp 8]()
-
![Đề thi học kì 1 Hóa lớp 8 năm 2016-2017]()
-
![Đề thi học kì 1 Hóa lớp 8]()
-
![Đề thi học kì 1 Hóa 8 trường THCS Thái Bình năm 2016-2017]()
-
![Đề thi học kì 1 Hóa 8 trường THCS Biên Giới năm 2016-2017]()
-
![Đề thi học kì 1 Hóa 8]()
-
![Đề thi học kì 1 Hóa 8 trường THCS Sơn Lâm năm 2021-2022]()
-
![Đề thi học kì 1 Hóa 8 năm 2020-2021]()
-
![Đề thi học kì 2 Hóa 8 trường PTDTBT THCS Liên xã La ÊÊ - Chơ Chun năm 2021-2022]()
Có thể bạn quan tâm
Thông tin tài liệu
Trường THCS An Ngãi Trung
ĐỀ KIỂM TRA HỌC KÌ I NĂM HỌC 2019-2020
Môn: Hóa học – Lớp 8
Thời gian: 45 phút
A- MỤC TIÊU
Kiến thức:
Kiểm tra kiến thức về
Chương 1
- Nguyên tử
- Nguyên tố hóa học – Đơn chất và hợp chất
- Công thức hóa học, hóa trị
Chương 2
- Phản ứng hóa học
- Định luật bảo toàn khối lượng
- Phương trình hóa học
Chương 3
- Mol – chuyển đổi giữa n, m, V
- Tỉ khối của chất khí
- Tính theo công thức hóa học
- Tính theo phương trình hóa học
Kĩ năng:
- Lập được công thức hóa học và lập được phương trình hóa học, tính được khối lượng của một chất
trong phản ứng khi biết khối lượng của các chất còn lại.
- Tính được khối lượng mol nguyên tử, mol pjân tử của các chất theo công thức.
- Tính được m (hoặc n, hoặc V) của chất khí ở điều kiện tiêu chuẩn khi biết đại lượng có liên quan.
- Tính được tỉ khối của khí A đối với khí B , đối với không khí.
- Tính được thành phần phần trăm về khối lượng của các nguyên tố khi biết công thức hóa học; Xác định
công thức hóa học khi biết thành phần phần trăm về khối lượng các nguyên tố tạo nên hợp chất
- Tính được tỉ lệ số mol giữa các chất theo phương trình hóa học cụ thể; Tính được khối lượng chất phản
ứng; Tính được thể tích chất khí tham gia hoặc tạo thành trong phản ứng.
Cấu trúc đề
Phần I : Trắc nghiệm: 12 câu (3 điểm) (15 phút)
Phần II: Tự luận 3 câu (7 điểm) (30 phút)
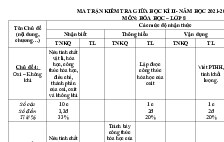
B. MA TRẬN ĐỀ
MỨC ĐỘ NHẬN THỨC
Nội dung
kiến thức
ChấtNguyên tửPhân tử
Số câu hỏi
Số điểm
Phản ứng
hoa học.
Số câu hỏi
Số điểm
Nhận biết
TN
TL
- Nhận biết được
một số tính chất của
chất. Khái niệm về
chất nguyên chất và
hỗn hợp.
- Nhận biết được
cấu tạo của nguyên
tử.
2
1
0,5
0,25
TN
TL
- Phân biệt được
đơn chất và hợp
chất.
- Tính được phân
tử khối của chất.
- Nhận biết được sự
biến đổi chất, sự
biến đổi thuộc hiện
tượng vật lí và hiện
tượng hóa học.
- Nhận biết được
chất tham gia và
chất sản phẩm.
3
1
0,75
0,5
- Biết áp dụng
được định luật bảo
toàn khối lượng để
tính khối lượng
của các chất.
- Biết cách lập
PTHH.
2
0,5
1
0,25
1
0,25
2
2
- Biết được cách
so sánh tỉ khối của
các chất với nhau,
tỉ khối của một
chất so với không
khí.
Mol và tính
toán hoá
học
Số câu hỏi
1
0,25
Vận dụng ở mức
độ cao hơn
TN
TL
Vận dụng
TN
TL
.Lập được công
thức hóa học của
một hợp chất.
1
0,25
CỘNG
7
1,75
17,5%
- Nêu được ý
nghĩa của PTHH.
- Viết được PTHH
của một phản ứng
hóa học.
1
0,25
.
1
0,5
- Tính được số mol
của một chất.
- Tìm thành phần
phần trăm của
nguyên tố khí biết
CTHH.
- Làm được bài tập
tính khối lượng,
thể tích của một
chất theo phương
trình hóa học.
- Giải được bài tập
xác định CTHH
của hợp chất khi
biết thành phần %
của các nguyên tố
trong hợp chất.
5 câu
2 Câu
4 câu
3 câu
3 câu
3 câu
1 câu
1,25 đ
0,75 đ
1đ
2,25 đ
0,75 đ
3đ
1đ
10 đ
20%
1
0,25
9
4,25 đ
42,5%
5
4
40%
21 câu
Số điểm
Tổng số
câu
Tổng số
điểm
Thông hiểu
32,5%
2
2,5
37,5%
1
1
10%
Trường THCS An Ngãi Trung
Lớp:….
Họ & tên:………………………
KIỂM TRA HỌC KÌ I NĂM HỌC 2019-2020
Môn: Hóa học– Lớp 8
Đề 1
Thời gian: 45 phút
I- TRẮC NGHIỆM (3 điểm)
Chọn một trong những phương án đúng trong các câu sau rồi ghi kết quả vào khung bên dưới:
1. Hạt nhân nguyên tử được tạo bởi
A. proton, nơtron.
B. proton, electron. C. electron.
D. electron, nơtron.
2. Tính chất nào sau đây cho ta biết đó là chất tinh khiết?
A. Không màu, không mùi.
B. Có vị ngọt, mặn hoặc chua.
C. Không tan trong nước.
D. Khi đun thấy sôi ở nhiệt độ xác định.
3. Cho các chất có công thức hóa học sau: Na, O3, CO2, Cl2, NaNO3, SO3. Dãy công thức gồm các hợp chất là
A. Na, O3, Cl2.
B. CO2, NaNO3, SO3.
C. Na, Cl2, CO2.
D. Na, Cl2, SO3.
4. Biết Ca (II) và PO4 (III) vậy công thức hóa học đúng là
A. CaPO4.
B. Ca3PO4.
C. Ca3(PO4)2.
D. Ca(PO4)2.
5. Hiện tượng nào là hiện tượng vật lí?
A. Đập đá vôi sắp vào lò nung.
B. Làm sữa chua.
C. Muối dưa cải.
D. Sắt bị gỉ.
6. Cho phương trình hóa học sau SO3 + H2O H2SO4. Chất tham gia là
A. SO3, H2SO4.
B. H2SO4.
C. H2O, H2SO4.
D. SO3, H2O.
7. Đốt cháy 12,8 g bột đồng trong không khí, thu được 16g đồng (II) oxit CuO. Khối lượng của oxi tham gia
phản ứng là
A. 1,6 g.
B. 3,2 g.
C. 6,4 g.
D. 28,8 g.
8. Khí lưu huỳnh đioxit SO2 nặng hay nhẹ hơn khí oxi bao nhiêu lần?
A. Nặng hơn 2 lần. B. Nặng hơn 4 lần. C. Nhẹ hơn 2 lần.
D. Nhẹ hơn 4 lần.
9. Phản ứng nào sau đây được cân bằng chưa đúng?
A. CaO + H2O Ca(OH)2.
B. S + O2 SO2.
C. NaOH + HCl NaCl + H2O.
D. Cu(OH)2 + 2HCl CuCl2 + H2O.
10. Số mol của 11,2 g Fe là
A. 0,1 mol.
B. 0,2 mol.
C. 0,21 mol.
D. 0,12 mol.
11. Để chỉ 3 phân tử Oxi ta viết
A. 3O.
B. O3.
C. 3O2.
D. 2O3.
12. Dãy chất nào sau đây chỉ kim loại?
A. Đồng, Bạc, Nhôm, Magie.
B. Sắt, Lưu huỳnh, Cacbon, Nhôm.
C. Cacbon, Lưu huỳnh, Photpho, Oxi.
D. Bạc, Oxi, Sắt, Nhôm.
Câu
1
2
3
4
5
6
7
8
9
10
11
12
Đáp án
II. TỰ LUẬN (7 điểm)
Câu 1(1 điểm): Nối cột A với nội dung ở cột B sao cho phù hợp.
A
B
Trả lời
1. Cồn để trong lọ không kín bị bay hơi.
a. chất tinh khiết.
………
2. Đốt than trong không khí.
b. 170 đvC.
………
3. AgNO3 có phân tử khối bằng
c. Hiện tượng vật lí.
………..
4. Nước cất là
d. Hiện tượng hóa học.
………
Câu 2 (2 điểm): Lập phương trình hóa học các phản ứng sau: ( làm trực tiếp vào đề)
a) Ba + O2
BaO.
c)
KClO3
KCl + O2.
b) Fe3O4 + CO
Fe + CO2.
d) Al + CuSO4
Al2(SO4)3 + Cu.
Câu 3 (3 điểm): Cho 4,8 g kim loại Magie tác dụng hết với dung dịch axit clohiđric HCl theo phương trình:
Mg + HCl
MgCl2 + H2.
a) Lập phương trình hóa học của phản ứng trên.
b) Tính khối lượng Magie clorua MgCl2 tạo thành.
c) Tính thể tích khí H2 sinh (ở đktc).
Câu 4 (1 điểm): Một oxit của lưu huỳnh có thành phần trăm của lưu huỳnh là 50% và Oxi là 50%. Biết oxit này
có khối lượng mol phân tử là 64 g/mol. Hãy tìm công thức hóa học của oxit đó.
Cho nguyên tử khối: O=16, Cu=64, Mg=24, Fe=56, Cl=35,5, Ag =108, N=14.
Trường THCS An Ngãi Trung
Lớp:….
Họ & tên:………………………
- HẾT KIỂM TRA HỌC KÌ I NĂM HỌC 2019-2020
Môn: Hóa học– Lớp 8
Đề 2
Thời gian: 45 phút
I- TRẮC NGHIỆM (3 điểm)
Chọn một trong những phương án đúng trong các câu sau rồi ghi kết quả vào khung bên dưới:
1. Hiện tượng nào là hiện tượng vật lí?
A. Đập đá vôi sắp vào lò nung.
B. Làm sữa chua.
C. Muối dưa cải.
D. Sắt bị gỉ.
2. Để chỉ 3 phân tử Oxi ta viết
A. 3O.
B. O3.
C. 3O2.
D. 2O3.
3. Hạt nhân nguyên tử được tạo bởi
A. proton, nơtron.
B. proton, electron. C. electron.
D. electron, nơtron.
4. Tính chất nào sau đây cho ta biết đó là chất tinh khiết?
A. Không màu, không mùi.
B. Có vị ngọt, mặn hoặc chua.
C. Không tan trong nước.
D. Khi đun thấy sôi ở nhiệt độ xác định.
5. Cho các chất có công thức hóa học sau: Na, O3, CO2, Cl2, NaNO3, SO3. Dãy công thức gồm các hợp chất là
A. Na, O3, Cl2.
B. CO2, NaNO3, SO3.
C. Na, Cl2, CO2.
D. Na, Cl2, SO3.
6. Phản ứng nào sau đây được cân bằng chưa đúng?
A. CaO + H2O Ca(OH)2.
B. S + O2 SO2.
C. NaOH + HCl NaCl + H2O.
D. Cu(OH)2 + 2HCl CuCl2 + H2O.
7. Dãy chất nào sau đây chỉ kim loại?
A. Đồng, Bạc, Nhôm, Magie.
B. Sắt, Lưu huỳnh, Cacbon, Nhôm.
C. Cacbon, Lưu huỳnh, Photpho, Oxi.
D. Bạc, Oxi, Sắt, Nhôm.
8. Khí lưu huỳnh đioxit SO2 nặng hay nhẹ hơn khí oxi bao nhiêu lần?
A. Nặng hơn 2 lần. B. Nặng hơn 4 lần. C. Nhẹ hơn 2 lần.
D. Nhẹ hơn 4 lần.
9. Cho phương trình hóa học sau SO3 + H2O H2SO4. Chất tham gia là
A. SO3, H2SO4.
B. H2SO4.
C. H2O, H2SO4.
D. SO3, H2O.
10. Biết Ca (II) và PO4 (III) vậy công thức hóa học đúng là
A. CaPO4.
B. Ca3PO4.
C. Ca3(PO4)2.
D. Ca(PO4)2.
11. Số mol của 11,2 g Fe là
A. 0,1 mol.
B. 0,2 mol.
C. 0,21 mol.
D. 0,12 mol.
12. Đốt cháy 12,8 g bột đồng trong không khí, thu được 16g đồng (II) oxit CuO. Khối lượng của oxi tham gia
phản ứng là
A. 1,6 g.
B. 3,2 g.
C. 6,4 g.
D. 28,8 g.
Câu
1
2
3
4
5
6
7
8
9
10
11
12
Đáp án
II. TỰ LUẬN (7 điểm)
Câu 1(1 điểm): Nối cột A với nội dung ở cột B sao cho phù hợp.
A
B
Trả lời
1. Cồn để trong lọ không kín bị bay hơi.
a. chất tinh khiết.
………
2. Đốt than trong không khí.
b. 170 đvC.
………
3. AgNO3 có phân tử khối bằng
c. Hiện tượng vật lí.
………..
4. Nước cất là
d. Hiện tượng hóa học.
………
Câu 2 (2 điểm): Lập phương trình hóa học các phản ứng sau: ( làm trực tiếp vào đề)
a) Ba + O2
BaO.
c)
KClO3
KCl + O2.
b) Fe3O4 + CO
Fe + CO2.
d) Al + CuSO4
Al2(SO4)3 + Cu.
Câu 3 (3 điểm): Cho 4,8 g kim loại Magie tác dụng hết với dung dịch axit clohiđric HCl theo phương trình:
Mg + HCl
MgCl2 + H2.
a) Lập phương trình hóa học của phản ứng trên.
b) Tính khối lượng Magie clorua MgCl2 tạo thành.
c) Tính thể tích khí H2 sinh (ở đktc).
Câu 4 (1 điểm): Một oxit của lưu huỳnh có thành phần trăm của lưu huỳnh là 50% và Oxi là 50%. Biết oxit này
có khối lượng mol phân tử là 64 g/mol. Hãy tìm công thức hóa học của oxit đó.
Cho nguyên tử khối: O=16, Cu=64, Mg=24, Fe=56, Cl=35,5, Ag =108, N=14.
- HẾT Trường THCS An Ngãi Trung
KIỂM TRA HỌC KÌ I NĂM HỌC 2019-2020
Môn: Hóa học– Lớp 8
Đề 1
Thời gian: 45 phút
HƯỚNG DẪN CHẤM
I- TRẮC NGHIỆM: 3 đ
Mỗi phương án trả lời đúng = 0,25 đ
Câu
Đáp án
1
A
2
D
3
B
4
C
5
A
6
D
7
B
8
A
9
D
10
B
II- TỰ LUẬN: 7 đ
Câu
Nội dung
1
Mỗi ý đúng 0,25 đ
1-c; 2-d; 3-b; 4-a
2
11
C
Điểm
1Đ
Mỗi PTHH được cân bằng đúng: 0,5 đ
a) 2Ba + O2 2BaO.
c) 2KClO3 2KCl + 3O2.
b) Fe3O4 + 4CO 3 Fe + 4CO2. d) 2Al + 3CuSO4 Al2(SO4)3 + 3Cu.
3
2Đ
3,0 Đ
Mg + 2HCl MgCl2 + H2
n Mg =
(1) ……………………………………………….
0,5 đ
0,5 đ
4,8
=0,2 (mol )
24
………………………………………………………..
0,5 đ
Theo (1): nH2 = nMgCl2 = nMg = 0,2 mol ………………………………………..
0,75 đ
Khối lượng Magie clorua MgCl2 tạo thành mMgCl2= 0,2. 95= 19 (g)……………
0,75 đ
Thể tích H2: VH2 = n.22,4 = 0,2.22,4 = 4,48 (lit)
.................................................
4
1Đ
Đặt CTHH: SxOy
32 x 16 y 64
=
=
50
100 .
Ta có: 50
Suy ra x=1; y =2
Vậy CTHH là SO2.
* Ghi chú Học sinh giải bằng phương pháp khác nếu đúng vẫn đạt điểm tối đa.
12
A
Trường THCS An Ngãi Trung
KIỂM TRA HỌC KÌ I NĂM HỌC 2019-2020
Môn: Hóa học– Lớp 8
Đề 2
Thời gian: 45 phút
HƯỚNG DẪN CHẤM
I- TRẮC NGHIỆM: 3 đ
Mỗi phương án trả lời đúng = 0,25 đ
Câu
Đáp án
1
A
2
C
3
A
4
D
5
B
6
D
7
A
8
A
9
D
10
C
II- TỰ LUẬN: 7 đ
Câu
Nội dung
1
Mỗi ý đúng 0,25 đ
1-c; 2-d; 3-b; 4-a
2
11
B
Điểm
1 Đ
Mỗi PTHH được cân bằng đúng: 0,5 đ
a) 2Ba + O2 2BaO.
b) Fe3O4 + 4CO 3 Fe + 4CO2.
2Đ
c) 2KClO3 2KCl + 3O2.
d) 2Al + 3CuSO4 Al2(SO4)3 + 3Cu.
3
3,0 Đ
Mg + 2HCl MgCl2 + H2
n Mg =
12
B
(1) ……………………………………………….
0,5 đ
0,5 đ
4,8
=0,2 (mol )
24
………………………………………………………..
0,5 đ
Theo (1): nH2 = nMgCl2 = nMg = 0,2 mol ………………………………………..
0,75 đ
Khối lượng Magie clorua MgCl2 tạo thành mMgCl2= 0,2. 95= 19 (g)……………
0,75 đ
Thể tích H2: VH2 = n.22,4 = 0,2.22,4 = 4,48 (lit)
.................................................
4
1Đ
Đặt CTHH: SxOy
32 x 16 y 64
=
=
50
100 .
Ta có: 50
Suy ra x=1; y =2
Vậy CTHH là SO2.
* Ghi chú Học sinh giải bằng phương pháp khác nếu đúng vẫn đạt điểm tối đa.