Đề thi học kì 2 Hóa 8 trường THCS Phú Lộc
Nội dung tài liệu
Tải xuống
Link tài liệu:
Các tài liệu liên quan
-
![Đề thi học kì 1 Hóa 8 trường THCS TT Vĩnh Tường năm 2017-2018]()
-
![Đề kiểm tra học kì 1 Hóa lớp 8]()
-
![Đề thi học kì 1 Hóa lớp 8 năm 2016-2017]()
-
![Đề thi học kì 1 Hóa lớp 8]()
-
![Đề thi học kì 1 Hóa 8 trường THCS Thái Bình năm 2016-2017]()
-
![Đề thi học kì 1 Hóa 8 trường THCS Biên Giới năm 2016-2017]()
-
![Đề thi học kì 1 Hóa 8]()
-
![Đề thi học kì 1 Hóa 8 trường THCS Sơn Lâm năm 2021-2022]()
-
![Đề thi học kì 1 Hóa 8 năm 2020-2021]()
-
![Đề thi học kì 2 Hóa 8 trường PTDTBT THCS Liên xã La ÊÊ - Chơ Chun năm 2021-2022]()
Có thể bạn quan tâm
Thông tin tài liệu
TRƯỜNG THCS PHÚ LỘC
KIỂM TRA HOÁ HỌC 8 TIẾT
46
Họ và tên: …………………..…… ………………………………. Lớp 8…
ĐỀA
Điểm
Lời phê của giáo viên
I Phần trắc nghiệm (2điểm)
Câu I:Điền đúng(Đ) sai (S) vào ô trống cuối ý mang nội dung đúng hoặc sai
tương ứng sau:
A.Oxit được chia làm hai loại chính là oxit axit và oxit bazơ.
B.Tất cả các oxit kim loại đều là oxit bazơ
C. Oxit của phi kim đều là oxit axit
D.Oxit axit thường là oxit cua phi kim và tương ứng với một axit.
E..Oxit bazơ là oxit của kim loại và tương ứng với một bazơ.
Câu II:Khoanh tròn vào chữ cái đứng trước câu trả lời đúng nhất.
1.Sự oxi hoá là :
A.Sự tác dụng của một chất với oxi .
B. Sự tác dụng của các chất với oxi.
C. Sự tác dụng của oxi với một chất.
D.Sự tác dụng của o xi với các chất.
2.Dãy các chất sau đều là oxit axit.
A.CO2 ,P2O5 ,H2O ,CaO.
B. CO2 ,P2O5 , SO3 ,N2O5 .
C.CO2 ,CaO ,CuO ,ZnO.
D.MgO , ZnO , CO , H2O2 .
3.Thành phần của không khí gồm :
A.21% N2 ,78% O2,1% khí khác
B. 21% O2 ,78% N2,1% khí khác
C. 1% N2 ,78% O2,21% khí khác
D.21% N2 ,1 % O2,78% khí khác
Phần tự luận: (8đ)
Câu III: So sánh sự cháy với sự o xi hóa chậm ? Cho ví dụ?
Câu IV:Với cùng khối lượng là a gam nguyên liệu điều chế O2 trong phòng thí
nghiệm KMnO4 , KClO3 thì chất nào điều chế được nhiều O2 hơn?Giải thích?
Câu IV: a.Để đốt cháy hết 2,4 gam than người ta dùng một thể tích oxi là bao
nhiêu? (biết thể tích oxi đo ở đktc).
b.Tính khối lượng kalipemangannat cần dùng để điều chế lượng oxi trên?
(nếu hiệu suất p/ứng đạt 90%)
BÀI LÀM
……………………………………………………………………………………
……………………………………………………………………………………
……………………………………………………………………………………
……………………………………………………………………………………
……………………………………………………………………………………
……………………………………………………………………………………
……………………………………………………………………………………
…………......................................................................................................
........................................
……………………………………………………………………………………
…………
TRƯỜNG THCS PHÚ LỘC
KIỂM TRA HOÁ HỌC 8 TIẾT
46
Họ và tên: …………………..…… ………………………………. Lớp 8…
ĐỀB
Điểm
Lời phê của giáo viên
I Phần trắc nghiệm (2điểm)
Câu I:Điền đúng(Đ) sai (S) vào ô trống cuối ý mang nội dung đúng hoặc sai
tương ứng sau: A.Oxit được chia làm hai loại chính là oxit axit và oxit bazơ.
B. Oxit bazơ là oxit của kim loại và tương ứng với một bazơ.
C.Tất cả các oxit của kim loại đều là oxit bazơ
D.Oxit axit thường là oxit cua phi kim và tương ứng với một axit.
E.Oxit của phi kim đều là oxit axit
Câu II:Khoanh tròn vào chữ cái đứng trước câu trả lời đúng nhất:
1.O xit là:
A.Hợp chất của hai nguyên tố
B.Hợp chất của ba nguyên tố.
C.Trong đó có một nguyên tố
D.Cả A và C.
2 Dãy các chất sau đều là oxit bazơ:
A.CO2 ,P2O5 ,H2O ,CaO.
B. CO2 ,P2O5 , SO3 ,N2O5 .
C.Fe2O3 ,CaO ,CuO ,ZnO.
D.MgO , ZnO , CO , H2O2 .
3.Sự o xi hóa là :
A. Sự tác dụng của một chất với oxi
B.Sự tác dụng của oxi với một chất
C. Sự tác dụng của nhiều chất với oxi
C.Sự tác dụng của oxi với nhiều
chất.
Phần tự luận: (8đ)
Câu III: Phân biệt phản ứng phân huỷ và phản ứng hoá hợp ? cho ví dụ?
Câu IV:Với cùng khối lượng là b gam nguyên liệu điều chế O2 trong phòng thí
nghiệm KMnO4 , KClO3 thì chất nào điều chế được nhiều O2 hơn?
Câu V: : a.Để đốt cháy hết 3,6 gam than người ta dùng một thể tích oxi là bao
nhiêu? (biết thể tích oxi đo ở đktc).
b.Tính khối lượng kaliclorat cần dùng để điều chế lượng oxi trên?.
(nếu hiệu suất phản ứng đạt 80%)
BÀI LÀM
……………………………………………………………………………………
……………………………………………………………………………………
……………………………………………………………………………………
……………………………………………………………………………………
……………………………………………………………………………………
……………………………………………………………………………………
……………………………………………………………………………………
…………......................................................................................................
...............................…
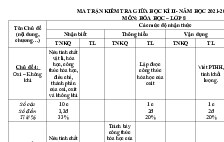
MA TRẬN ĐỀ KIỂM TRA HOÁ 8 TIẾT 46
MỨC ĐỘ NHẬN THỨC
NỘI DUNG
BIẾT
TNKQ
tính chất hoá học
của oxi
Oxit,oxi hoá
HIỂU
TL
Không khí sự cháy
Tổng
TL
TNKQ
2
2,5đ
2đ
2
4
4,5đ
1
0,5đ
3
1đ
2
1
0.5đ
1,5đ
2
0.5đ
2
TRỌNG
SỐ
TL
2
Phản ứng hoá hợp
p/ư phân huỷ.
đ/c ,ứng dụng của
oxi
TNKQ
VẬN DỤNG
4
1đ
1,5đ
1
1đ
4
0,5đ
2đ
2
2
0,5đ
6
0.5đ
3
1.5đ
2
3.5đ
4
0.5đ
2
2.5đ
17
2đ
10đ
ĐÁP ÁN VÀ BIỂU CHẤM
ĐỀ A
PHẦN TRẮC NGHIỆM: Câu I:
A:Đ; B:S; C:S; D:Đ;
E:Đ.
Câu II:
1C ; 2B ; 3B.
ĐỀ B
Câu I:
A:Đ; B:Đ; C:S; D:Đ;
E:S.
Câu II:
1D ; 2C ;3B
PHẦN TỰ LUẬN:
Câu III: Giống nhau : Đều là sự oxi hóa ,có tỏa nhiệt .
Khác nhau : Sự cháy có phát sáng còn sự oxi hóa chậm không phát sáng.
Ví dụ : Sự cháy : ga cháy ,than cháy...
Sự oxi hóa chậm :cửa sắt để lâu trong không khí bị oxi hoá.
Câu IV: Số mol của KClO3 là : a/122,5 mol
Số mol của KMnO4 : a/158 mol.
PTHH:
2KClO3 ->
KCl + 3O2 (1)
1mol :
1mol :
3mol
a/122,5
:3a/122,5
Theo PTHH : noxi = 2/3nKaliclorat=3a/122,5mol.
PTHH:
2KMnO4 -> K2MnO4 + MnO2 + O2. (2)
2mol
:1mol
a/158 mol
: a/2.158 mol.
Theo PTHH: noxi = 1/2nKalipemangannat= a/2.158 mol.
Ta có : 3a/122,5mol> a/2.158 mol.
Vậy với cùng một lượng a g nguyên liệu thì KClO3 cho nhiều oxi hơn KMnO4 .
Câu IV: a. Số mol của than là: 2,4/12= 0,2 mol.
PTHH:
C + O2 -> CO2
(1)
1mol: 1mol
Theo PTHH ta có : nOxi = nC = 0,2 mol
Thể tích của oxi là :0,2.22,4 = 4,48 lit
b. PTHH :
2KMnO4 -> K2MnO4 + MnO2 + O2. (2)
2mol
: 1mol
?
: 0,2mol
Theo PTHH : nKMnO 4 = 2nO 2 = 0,2.2=0,4 mol
Kl của KMnO4 theo PTHH là:0,4.158=63,2 g .
Do hiêu suất chỉ đạt 90% nên lượng nguyên liệu cần dùng nhiều hơn thực tế:
63,2.100/90= 70,22 g