Đề thi học kì 2 Hóa 8 trường THCS Nguyễn Văn Ẩn năm 2018-2019
Nội dung tài liệu
Tải xuống
Link tài liệu:
Các tài liệu liên quan
-
![Đề thi học kì 1 Hóa 8 trường THCS TT Vĩnh Tường năm 2017-2018]()
-
![Đề kiểm tra học kì 1 Hóa lớp 8]()
-
![Đề thi học kì 1 Hóa lớp 8 năm 2016-2017]()
-
![Đề thi học kì 1 Hóa lớp 8]()
-
![Đề thi học kì 1 Hóa 8 trường THCS Thái Bình năm 2016-2017]()
-
![Đề thi học kì 1 Hóa 8 trường THCS Biên Giới năm 2016-2017]()
-
![Đề thi học kì 1 Hóa 8]()
-
![Đề thi học kì 1 Hóa 8 trường THCS Sơn Lâm năm 2021-2022]()
-
![Đề thi học kì 1 Hóa 8 năm 2020-2021]()
-
![Đề thi học kì 2 Hóa 8 trường PTDTBT THCS Liên xã La ÊÊ - Chơ Chun năm 2021-2022]()
Có thể bạn quan tâm
Thông tin tài liệu
PHÒNG GD-ĐT BẾN CẦU
TRƯỜNG THCS NGUYỄN VĂN ẨN
ĐỀ KIỂM TRA HỌC KÌ II
NĂM HỌC 2018- 2019
MÔN: HÓA HỌC 8
THỜI GIAN: 45 phút
(Không tính thời gian viết đề )
ĐỀ
Câu 1: Oxit là gì? Có mấy loại oxit, kể ra? (1đ)
Câu 2 Cho các loại oxit sau: CO2, FeO, P2O5, Na2O, ZnO, CuO, SO3 , SiO2 .
- Hãy phân loại chúng . (1đ)
Câu 3: Hãy lập các phương trình hóa học của các phản ứng có sơ đồ sau và cho
biết mỗi phản ứng thuộc loại nào: (2đ)
a.
S +
O2
--SO2
b.
P
+
c.
KMnO4
d.
Fe
+
O2
-----
CuCl2
P2O5
K2MnO4
---
FeCl2
+
MnO 2 + O2
+
Câu 4:
a. Muối là gì, muối được phân làm mấy loại ?
Cu
(1đ)
b. Hãy đọc tên các chất sau: NaCl, K2SO4 , NaH2PO4 , Na2HPO4
(1đ)
Câu 5: Hãy viết công thức tính nồng độ mol của dung dịch. Ghi rõ tên, đơn vị mỗi
đại lương trong công thức? (1đ)
Câu 6: Tính số mol và số gam chất tan có trong 2.5 lít dung dịch CaCl 2 0.1 M.
(2đ)
( Cho Ca= 40; Cl = 35.5 ).
Duyệt của tổ trưởng
Long Thuận, ngày 23/04/2019
GVBM
Lâm Thị Phượng
Lê Thị Kim Nhàn
PHÒNG GD-ĐT BẾN CẦU
TRƯỜNG THCS NGUYỄN VĂN ẨN
ĐÁP ÁN KIỂM TRA HỌC KÌ II
NĂM HỌC 2018- 2019
MÔN: CÔNG NGHỆ 6
CÂU
ĐÁP ÁN
1
-Oxit là hợp chất của 2 nguyên tố, trong đó có một nguyên tố là oxi.
-Có 2 loại oxit: oxit axit và oxit bazơ.
0.5
0.5
2
- Oxit axit : CO2, P2O5, SO3 , SiO2
0.5
3
- Oxit bazơ: FeO, Na2O, ZnO, CuO,
a. S + O2
SO2 (PƯ hóa hợp)
0,5
0,75
b. 4P
0,75
+
5O2
c. 2KMnO4
d. Fe
4
+
2P2O5
ĐIỂM
(PƯ hóa hợp)
K2MnO4 + MnO 2 + O2 (PƯ phân hủy)
CuCl2
FeCl2 +
Cu (PƯ thế)
0.75
0.75
a.- Muối là hợp chất mà phân tử gồm có một hay nhiều nguyên tử 0,5
kim loại liên kết với một hay nhiều gốc axit.
- Muối được phân làm 2 loại là: muối trung hòa và muối axit
4
5
b.NaCl: Natriclorua
0.25
K2SO4 : kali sunfat
0.25
NaH2PO4: Natri đihidrophotphat
0.25
Na2HPO4 : Natri hidrophotphat
0.25
CM =
Trong đó:
.CM : Nồng độ mol của dung dịch (M)
.n : Số mol chất tan (mol)
.V : Thể tích dung dịch (l)
6
0,5
Số mol CaCl2 : nCaCl2 = 0,1 .2,5 = 0,25
(mol)
Số gam CaCl2 : mCaCl2 =0,25. 111= 27,75 (g)
0.5
0.5
1
1
Duyệt của tổ trưởng
Long Thuận, ngày 23/04/2019
GVBM
Lâm Thị Phượng
Lê Thị Kim Nhàn
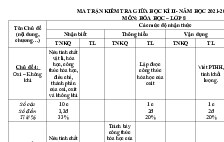
MA TRẬN:
TÊN CHỦ ĐỀ
NHẬN BIẾT
THÔNG
HIỂU
I. Oxi-không khí.
ĐN và phân loại
oxit
Phân loại oxit
Số câu
Số điểm
Câu 1
1
Câu 2
1
Tỉ lệ
10%
VẬN DỤNG
THẤP
VẬN DỤNG
CAO
TỔNG
2
10%
2
II. Axit- bazơ-muối
ĐN, phân loại
muối.
Đọc tên muối
Số câu
Số điểm
Câu 4a
1
Câu 4b
1
10%
Tỉ lệ
10%
2
2
III.Lập PTHH và
phân biệt các loại
phản ứng.
Phân biệt các
loại phản ứng
Lập PTHH
Số câu
Số điểm
Câu 3
Câu 3
20%
20%
2
Tỉ lệ
1
10%
2
20%
2
IV. Bài tập tính
theo PTHH và
Nồng độ dung dịch
Viết công thức
tính nồng độ
dung dịch.
Từ nồng độ dd,
tính số mol và số
gam chất tan.
Số câu
Số điểm
Câu 5
1
Câu 6
2
Tỉ lệ
Tổng số câu
Tổng số điểm
Tỉ lệ
3
3
30%
Duyệt của tổ trưởng
10%
3
3
30%
1
2
20%
20%
1
2
20%
8
10
100%
Long Thuận, ngày 23/04/2019
GVBM
Lâm Thị Phượng
Lê Thị Kim Nhàn
2
4
20%
40 %
Tuần dạy : 34
Tiết : 65
Ngày dạy:
KIỂM TRA HỌC KÌ II
1. Mục tiêu:
1.1. Kiến thức:
Củng cố : Về tính chất vật lí và tính chất hóa học của oxi, hidro, nước. Khái niệm phản ứng hóa
hợp, phân hủy và phản ứng thế.
1.2. Kĩ năng:
-Phân biệt các loại phản ứng hóa học; phân biệt và gọi tên oxít, axít, bazơ, muối
- Giải được bài toán tính theo PTHH.
1.3. Thái độ:
- Giáo dục tính cẩn thận, chính xác, nghiêm túc, trật tự khi làm bài kiểm tra
II. Ma trận đề kiểm tra:
TÊN CHỦ ĐỀ
NHẬN BIẾT
THÔNG
HIỂU
I. Oxi-không khí.
ĐN và phân loại
oxit
Phân loại oxit
Số câu
Số điểm
Câu 1
1
Câu 2
1
Tỉ lệ
10%
VẬN DỤNG
THẤP
VẬN DỤNG
CAO
TỔNG
2
10%
2
II. Axit- bazơ-muối
ĐN, phân loại
muối.
Đọc tên muối
Số câu
Số điểm
Câu 4a
1
Câu 4b
1
10%
Tỉ lệ
10%
2
2
III.Lập PTHH và
phân biệt các loại
phản ứng.
Phân biệt các
loại phản ứng
Lập PTHH
Số câu
Số điểm
Câu 3
Câu 3
20%
20%
2
Tỉ lệ
1
IV. Bài tập tính
theo PTHH và
Nồng độ dung dịch
Viết công thức
tính nồng độ
dung dịch.
10%
2
20%
2
Từ nồng độ dd,
tính số mol và số
gam chất tan.
20%
Số câu
Số điểm
Câu 5
1
Tỉ lệ
Tổng số câu
Tổng số điểm
Tỉ lệ
Câu 6
2
10%
3
3
30%
3
3
30%
1
2
20%
2
4
20%
1
2
20%
40 %
8
10
100%
III. Đề kiểm tra:
Câu 1: Oxit là gì? Có mấy loại oxit, kể ra? (1đ)
Câu 2 Cho các loại oxit sau: CO2, FeO, P2O5, Na2O, ZnO, CuO, SO3 , SiO2
.- Hãy phân loại chúng . (1đ)
Câu 3: Hãy lập các phương trình hóa học của các phản ứng có sơ đồ sau và cho biết mỗi phản
ứng thuộc loại nào: (3đ)
a.
S + O2
--SO2
b.
P
c.
d.
+
O2
KMnO4
---
P2O5
---
Fe + CuCl2
K2MnO4
---
+
MnO 2 + O2
FeCl2
+
Cu
Câu 4:
c. Muối là gì, muối được phân làm mấy loại ?
(1đ)
d. Hãy đọc tên các chất sau: NaCl, K2SO4 , NaH2PO4 , Na2HPO4
(1đ)
Câu 5: Hãy viết công thức tính nồng độ mol của dung dịch. Ghi rõ tên, đơn vị mỗi đại lương
trong công thức? (1đ)
Câu 6: Tính số mol và số gam chất tan có trong 2.5 lít dung dịch CaCl2 0.1 M.
(2đ)
( Cho Ca= 40; Cl = 35.5 ).
IV.Đáp án:
CÂU
1
ĐÁP ÁN
ĐIỂM
2
-Oxit là hợp chất của 2 nguyên tố, trong đó có một nguyên tố là
oxi.
-Có 2 loại oxit: oxit axit và oxit bazơ.
1
- Oxit axit : CO2, P2O5, SO3 , SiO2
0,5
3
- Oxit bazơ: FeO, Na2O, ZnO, CuO,
a. S +
O2
--SO2
b. P
4
+
O2
---
P2O5
(PƯ hóa hợp)
(PƯ hóa hợp)
c. KMnO4 ---
K2MnO4 + MnO 2 + O2 (PƯ phân hủy)
d. Fe +
---
CuCl2
FeCl2 + Cu (PƯ thế)
0,5
0,75
0,75
0.75
0.75
a.- Muối là hợp chất mà phân tử gồm có một hay nhiều nguyên 0,5
tử kim loại liên kết với một hay nhiều gốc axit.
- Muối được phân làm 2 loại là: muối trung hòa và muối axit
4
5
b.NaCl: Natriclorua
0.25
K2SO4 : kali sunfat
0.25
NaH2PO4: Natri đihidrophotphat
0.25
Na2HPO4 : Natri hidrophotphat
0.25
CM =
0.5
Trong đó:
.CM : Nồng độ mol của dung dịch (M)
.n : Số mol chất tan (mol)
.V : Thể tích dung dịch (l)
6
0,5
0.5
Số mol CaCl2 : nCaCl2 = 0,1 .2,5 = 0,25
(mol)
Số gam CaCl2 : mCaCl2 =0,25. 111= 27,75 (g)
1
1
V. Thống kê kết quả:
LỚP
8.1
8.2
8.3
8.4
TSHS
0-2
2-3,5
3,5-D5 CỘNG
% 5-D.6,5
6,5-D8
8-10
CỘNG %
Rút kinh nghiệm:
............................................................................................................................................................
........................................................................................................................
............................................................................................................................................................
........................................................................................................................