Đề thi học kì 2 Hóa 8 trường THCS Minh Tân năm 2019-2020
Nội dung tài liệu
Tải xuống
Link tài liệu:
Các tài liệu liên quan
-
![Đề thi học kì 1 Hóa 8 trường THCS TT Vĩnh Tường năm 2017-2018]()
-
![Đề kiểm tra học kì 1 Hóa lớp 8]()
-
![Đề thi học kì 1 Hóa lớp 8 năm 2016-2017]()
-
![Đề thi học kì 1 Hóa lớp 8]()
-
![Đề thi học kì 1 Hóa 8 trường THCS Thái Bình năm 2016-2017]()
-
![Đề thi học kì 1 Hóa 8 trường THCS Biên Giới năm 2016-2017]()
-
![Đề thi học kì 1 Hóa 8]()
-
![Đề thi học kì 1 Hóa 8 trường THCS Sơn Lâm năm 2021-2022]()
-
![Đề thi học kì 1 Hóa 8 năm 2020-2021]()
-
![Đề thi học kì 2 Hóa 8 trường PTDTBT THCS Liên xã La ÊÊ - Chơ Chun năm 2021-2022]()
Có thể bạn quan tâm
Thông tin tài liệu
TRƯỜNG THCS MINH TÂN
TỔ KHOA HỌC TỰ NHIÊN
KIỂM TRA HỌC KỲ II
Năm học 2019 - 2020
MÔN: HÓA HỌC 8
Tiết: 70
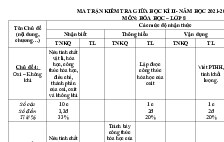
A. MA TRẬN
Mức độ
Chủ đề
1. Oxi –
Không
khí
2. Hidro
– Nước
3. Dung
dịch
Biết
TN
-Phương
pháp điều
chế khí oxi.
- Phân biệt
được oxit
axit và oxit
bazơ
-Thành
phần của
không khí
4
1,6
- Biết được
tính chất
của hidro.
- Tính chất
hóa học của
nước.
4
1,6
- Khái niệm
dung dịch,
độ tan,
công thức
tính nồng
độ phần
trăm, nồng
độ mol
2
10
Tổng
0,8
4
40
%
Hiểu
TL
TN
- Phân
biệt
được
phản
ứng
phân
hủy,
phản
ứng hóa
hợp
2 0,8
-Biết
các chất
tác
dụng
với
nước
-Gọi tên
các loại
hợp chấ
vô cơ
2 0,8
-Tính
được
khối
lượng
chất tan
trong
dung
dịch khi
biết
nồng độ
1 0,4
5
2
20
%
TL
-Viết
các
phương
trình
phản
ứng của
hidro và
nước
1
2
Vận dụng
Vận dụng thấp
Vận dụng cao
TN
TL
TN
TL
-Viết
được
phương
trình phản
ứng của
oxi với
các chất
1
2
-Tính
được thể
tích khí
và khối
lượng sản
phẩm tạo
thành,
tính được
nồng độ
phần trăm
1
1
Tổng
TN
TL
6
2,4
1
2
6
2,4
2
3
3
15
1,2
6
60
%
1
3
1
4
40
%
- Tính
toán và
pha chế
dung dich
theo nồng
độ cho
trước.
1
2
20
%
2
3
30
%
1
1
1
1
10
%
B. ĐỀ
PHẦN I: TRẮC NGHIỆM KHÁCH QUAN (6,0 điểm )
Khoanh tròn vào một chữ cái đứng đầu câu trả lời mà em cho là đúng
Câu 1: Nhiệt phân các chất KClO3, KMnO4 ở nhiệt độ cao là phương pháp điều chế khí nào
trong phòng thí nghiệm?
A. Khí oxi
B. Khí hidro
C. Khí nitơ
D. Cả A. B. C.
Câu 2: Khí nào nhẹ nhất trong các chất khí sau:
A. O2
B. H2
C. CO2
D. N2
Câu 3: Phản ứng hóa học sau thuộc loại phản ứng hóa học nào?
Na2CO3 + CO2 + H2O 2NaHCO3
A. Phản ứng hóa hợp
B. Phản ứng phân hủy
C. Phản ứng thế
D. Phản ứng oxi hóa – khử
Câu 4: Dãy các hợp chất sau: CaO, NO, CO2, Fe2O3, P2O5 thuộc loại hợp chất nào?
A. Axit
B. Oxit
C. Bazơ
D. Muối
Câu 5: Cho các chất có công thức hóa học sau: HCl , CO2 , H3PO4 , P2O5 , CaO , HNO3 ,
Mg(OH)2 , CuSO4 , Al2O3. Số các hợp chất là oxit là:
A. 2
B. 3
C. 4
D. 5
Câu 6: Phản ứng hóa học nào là phản ứng phân hủy trong các phản ứng sau?
A. Zn + 2HCl ZnCl2 + H2
B. CO2 + CaO CaCO3
C. NaOH + HCl NaCl + H2O
D. 2NaHCO3 Na2CO3 + CO2+H2O
Câu 7: Công thức tính nồng độ phần trăm của dung dịch là:
A. C %
mct .mdd
100%
B. C %
mct
.100%
mdd
C. C %
mct .mnuoc
100%
D. C %
mct mdd
100%
Câu 8: Trong các chất sau: Na, P2O5, CaO, Na2O. Nước tác dụng được với chất nào tạo ra
axit?
A. Na
B. P2O5
C. CaO
D. Na2O
0
Câu 9: Ở 20 C, hòa tan 20,7g CuSO4 vào 100g nước thì được một dung dịch CuSO4 bão
hòa. Vậy độ tan của CuSO4 trong nước ở 200C là:
A. 20g
B. 20,7g
C. 100g
D. 120,7g
Câu 10: Hòa tan hoàn toàn 10g đường vào 190g nước thì thu được dung dịch nước đường
có nồng độ bằng
A. 5,26%
B. 5,0%
C. 10%
D. 20%
Câu 11: Công thức tính nồng độ mol của dung dịch là:
A.
B.
C.
D.
Câu 12: Khối lượng chất tan NaOH có trong 100ml dung dịch NaOH 1,5M là: (Cho Na
=23, O=16, H=1)
A. 6g
B. 1,5g
C. 8g
D. 6000g
Câu 13: Chọn câu trả lời đúng trong các câu sau đây về thành phần thể tích của không khí.
A. 21% khí oxi, 78% khí nitơ, 1% các khí khác (CO2, CO, khí hiếm,…)
B. 21% các khí khác, 78% khí nitơ, 1% khí oxi.
C. 21% khí nitơ, 78% khí oxi, 1% các khí khác (CO2, CO, khí hiếm,…)
D. 21% khí oxi, 78% các khí khác, 1% khí nitơ.
Câu 14: Khi giảm nhiệt độ và tăng áp suất thì độ tan của chất khí trong nước:
A. đều tăng
B. đều giảm
C. có thể tăng và có thể giảm
D. không tăng và cũng không giảm
Câu 15: Dung dịch là hỗn hợp:
A. của chất rắn trong chất lỏng
B. của hai chất lỏng
C. của nước và chất lỏng
D. đồng nhất của dung môi và chất tan.
PHẦN II: TỰ LUẬN (4,0 điểm)
Câu 1 (1,0 điểm). Lập phương trình hóa học cho các sơ đồ phản ứng sau:
(Chú ý: Các em có thể điền trực tiếp vào chỗ (…….) sau và cân bằng sơ đồ)
1,
S
+
………
SO2
2,
CuO +
H2
……… +
H2O
3,
Na
+
H2O
……… +
H2
4,
CO2 +
H 2O
………
5,
Na2O +
……… NaOH
Câu 2 (1,0 điểm). Viết phương trình phản ứng khi cho các chất sau: S, P đỏ tác dụng với khí
oxi ở nhiệt độ cao.
Câu 3 (1,0 điểm). Cho 4,6 gam kim loại natri tác dụng hết với nước.
1. Viết phương trình phản ứng xảy ra.
2. Tính thể tích khí H2 thu được (ở đktc)
3. Tính khối lượng bazơ tạo thành sau phản ứng.
4. Tính nồng độ phần trăm của dung dịch bazơ thu được sau phản ứng.
Câu 4 (1,0 điểm). Nước muối sinh lí là dung dịch NaCl có nồng độ 0,9%. Nước muối sinh
lý đem lại khá nhiều lợi ích cho sức khỏe con người như dùng để làm sạch vết thương, loại
bỏ chất bẩn; dùng cho mũi họng; khi viêm răng miệng, viêm họng, đờm nhiều, miệng hôi,
súc miệng bằng nước muối sinh lý có thể giúp bạn tạo môi trường khoang miệng sạch sẽ,
nhanh khỏi bệnh hơn rất nhiều….. Nước muối sinh lí có thể dùng nước muối sinh lý cho
mọi lứa tuổi, kể cả em bé sơ sinh, trẻ nhỏ và phụ nữ có thai.
Vậy từ NaCl, nước cất và các dụng cụ cần thiết khác em hãy tính toán và nêu cách pha chế
500 gam dung dịch nước muối sinh lí NaCl 0,9%.
(Cho Na = 23, Fe =56, Zn = 65, Mg = 24, Cu = 64, H =1, O=16)
C. HƯỚNG DẪN CHẤM
PHẦN I: TRẮC NGHIỆM (6,0 điểm)
Mỗi ý đúng được 0,4 điểm
Câu
1
2
3
4
5
6
7
8
9 10
Đáp án
A
B
A
B
C D B B B
B
PHẦN II: TỰ LUẬN (4,0 điểm)
Câu
Hướng dẫn chấm
Câu 1
Mỗi phương trình đúng được 0,4 điểm
(1,0 điểm)
1,
S
+
O2
→ SO2
2,
CuO +
H2
→ Cu
3,
2Na
+
2H2O → 2NaOH
4,
CO2 +
H2O → H2CO3
5,
Na2O + H2O → 2NaOH
Câu 2
Mỗi phương trình đúng được 0,5 điểm
(1,0 điểm)
1,
S
+
O2
→ SO2
2,
4P
+ 5O2
→ 2P2O5
Không cân bằng phương trình chỉ được 0,3 điểm.
Câu 3
1. Số mol Na tham gia phản ứng là:
(1,0 điểm)
PT:
2Na + 2H2O 2NaOH +
Theo PT: 2 mol
2 mol
2mol
Theo ĐB: 0,2 mol
0,2 mol
0,2 mol
Vậy ta có:
2. Vậy thể tích khí H2 thu được ở đktc:
11
A
12
A
13
A
14
A
15
D
Điểm
+
+
H2O
H2
0,2 điểm
0,2 điểm
0,2 điểm
0,2 điểm
0,2 điểm
0,5 điểm
0,5 điểm
0,2 điểm
H2
1 mol
0,1 mol
3. Theo PT:
Vậy khối lượng của NaOH:
4. Khối lượng dung dịch thu được sau phản ứng:
mdd = mnước + mNa - mkhí hidro = 200 + 6,9 – 0,3 = 206,6 (gam)
Nồng độ phần trăm của dung dịch sau phản ứng là:
0,2 điểm
0,2 điểm
0,2 điểm
0,2 điểm
Câu 4
(1,0 điểm)
* Tính toán:
- Khối lượng NaCl có trong 500 gam dung dịch NaCl 0,9% là:
0,5 điểm
- Khối lượng nước cần dùng cho sự pha chế là:
*Cách pha chế: Cân lấy 4,5 gam NaCl rồi cho vào cốc có dung
tích 750ml. Cân lấy 495,5 gam nước (hoặc đong lấy 495,5ml
nước) cất, rồi đổ dần vào cốc và khuấy nhẹ. Được 500 gam dung
dịch NaCl 0,9%.
0,5 điểm
---------------- Hết ---------------Minh Tân, ngày 16 /02 /2020
BAN GIÁM HIỆU DUYỆT
Ngày
/
/2020
TỔ CHUYÊN MÔN
Ngày / /2020
NGƯỜI RA ĐỀ
Tổ trưởng
Trần Quốc Đương
Ký duyệt ngày
/2020
/
Trần Thế Hải
TRƯỜNG THCS MINH TÂN
Họ tên:..................................................
Lớp: 9.......
Điểm
Thứ
, ngày
tháng
năm 2020
KIỂM TRA HỌC KỲ II HÓA HỌC 8
Thời gian: 45 phút
Lời phê của thầy (cô)
giáo
..............................................................................................................
..............................................................................................................
..............................................................................................................
MÃ ĐỀ: 861
PHẦN I: TRẮC NGHIỆM KHÁCH QUAN (6,0 điểm )
Khoanh tròn vào một chữ cái đứng đầu câu trả lời mà em cho là đúng
Câu 1: Nhiệt phân các chất KClO3, KMnO4 ở nhiệt độ cao là phương pháp điều chế khí nào
trong phòng thí nghiệm?
A. Khí oxi
B. Khí hidro
C. Khí nitơ
D. Cả A. B. C.
Câu 2: Khí nào nhẹ nhất trong các chất khí sau:
A. O2
B. H2
C. CO2
D. N2
Câu 3: Phản ứng hóa học sau thuộc loại phản ứng hóa học nào?
Na2CO3 + CO2 + H2O 2NaHCO3
A. Phản ứng hóa hợp
B. Phản ứng phân hủy
C. Phản ứng thế
D. Phản ứng oxi hóa – khử
Câu 4: Dãy các hợp chất sau: CaO, NO, CO2, Fe2O3, P2O5 thuộc loại hợp chất nào?
A. Axit
B. Oxit
C. Bazơ
D. Muối
Câu 5: Cho các chất có công thức hóa học sau: HCl, CO2, H3PO4, NaOH, CaO, HNO3,
Mg(OH)2, CuSO4, H2CO3. Số các hợp chất là axit là:
A. 2
B. 3
C. 4
D. 5
Câu 6: Phản ứng hóa học nào là phản ứng phân hủy trong các phản ứng sau?
A. Zn + 2HCl ZnCl2 + H2
B. CO2 + CaO CaCO3
C. NaOH + HCl NaCl + H2O
D. 2NaHCO3 Na2CO3 + CO2+H2O
Câu 7: Công thức tính nồng độ phần trăm của dung dịch là:
A. C %
mct .mdd
100%
B. C %
mct
.100%
mdd
C. C %
mct .mnuoc
100%
D. C %
mct mdd
100%
Câu 8: Trong các chất sau: Na, P2O5, CaO, Na2O. Nước tác dụng được với chất nào tạo ra
axit?
A. Na
B. P2O5
C. CaO
D. Na2O
0
Câu 9: Ở 20 C, hòa tan 20,7g CuSO4 vào 100g nước thì được một dung dịch CuSO4 bão
hòa. Vậy độ tan của CuSO4 trong nước ở 200C là:
A. 20g
B. 20,7g
C. 100g
D. 120,7g
Câu 10: Hòa tan hoàn toàn 10g đường vào 190g nước thì thu được dung dịch nước đường
có nồng độ bằng
A. 5,26%
B. 5,0%
C. 10%
D. 20%
Câu 11: Chất nào là bazơ trong các chất có công thức hóa học sau:
A. Fe(OH)3
B. H2CO3
C. Ca(NO3)2
D. P2O5
Câu 12: Khối lượng chất tan NaOH có trong 100ml dung dịch NaOH 1,5M là: (Cho Na
=23, O=16, H=1)
A. 6g
B. 1,5g
C. 8g
D. 6000g
Câu 13: Chọn câu trả lời đúng trong các câu sau đây về thành phần thể tích của không khí.
A. 21% khí oxi, 78% khí nitơ, 1% các khí khác (CO2, CO, khí hiếm,…)
B. 21% các khí khác, 78% khí nitơ, 1% khí oxi.
C. 21% khí nitơ, 78% khí oxi, 1% các khí khác (CO2, CO, khí hiếm,…)
D. 21% khí oxi, 78% các khí khác, 1% khí nitơ.
Câu 14: Khi giảm nhiệt độ và tăng áp suất thì độ tan của chất khí trong nước:
A. đều tăng
B. đều giảm
C. có thể tăng và có thể giảm
D. không tăng và cũng không giảm
Câu 15: Dung dịch là hỗn hợp:
A. của chất rắn trong chất lỏng
B. của hai chất lỏng
C. của nước và chất lỏng
D. đồng nhất của dung môi và chất tan.
PHẦN II: TỰ LUẬN (4,0 điểm)
Câu 1 (1,5 điểm). Cho các chất sau: CaO, Na, SO2 tác dụng với nước. Viết các phương
trình phản ứng xảy ra.
Câu 2 (1,0 điểm). Có 3 lọ không nhãn đựng ba chất lỏng không màu sau:
HCl, NaOH, H2O
Bằng phương pháp hóa học nêu cách nhận biết 3 lọ đựng chất lỏng trên.
Câu 3 (1,5 điểm). Cho 6,9 gam kim loại natri tác dụng hết với nước.
A. Viết phương trình phản ứng xảy ra.
B. Tính thể tích khí H2 thu được (ở đktc)
C. Tính khối lượng bazơ tạo thành sau phản ứng.
D. Tính nồng độ phần trăm của dung dịch bazơ tạo thành sau phản ứng nếu khối lượng nước
tham gia phản ứng là 200 gam.
(Cho Na = 23, Fe =56, Zn = 65, Mg = 24, Cu = 64, H =1, O=16)
---------------- Bài làm ---------------…………………………………………………………………………………………
…………………………………………………………………………………………
…………………………………………………………………………………………
…………………………………………………………………………………………
…………………………………………………………………………………………
…………………………………………………………………………………………
…………………………………………………………………………………………
…………………………………………………………………………………………
…………………………………………………………………………………………
…………………………………………………………………………………………
…………………………………………………………………………………………
…………………………………………………………………………………………
…………………………………………………………………………………………
…………………………………………………………………………………………