Lý thuyết và Phương pháp giải
- Với dung dịch HCl, H2SO4 loãng
Kim loại trong cặp oxi hóa – khử có thế điện cực chuẩn âm (tức kim loại đứng trước H trong dãy hoạt động hóa học của kim loại) khử được ion hidro H+ của axit thành H2
- Với H2SO4 đặc nóng, HNO3: Hầu hết các kim loại (trừ Au, Pt) khử được S6+ và N5+ trong các axit này xuống số oxi hóa thấp hơn.
Chú ý: Nếu hỗn hợp kim loại tác dụng với hỗn hợp nhiều axit, nên viết phương trình phản ứng dạng chung (phương pháp chuyển bài toán hỗn hợp về chất tương đương) hay viết phản ứng dạng ion; viết các quá trình oxi hóa, quá trình khử, rồi vận dụng định luật bảo toàn khối lượng, bảo toàn electron để giải.
Các kiểu bài thường gặp
+) Kim loại tác dụng với 1 axit
+) Hỗn hợp kim loại tác dụng với 1 axit
+) Kim loại tác dụng với hỗn hợp axit
+) Hỗn hợp kim loại tác dụng vưới hỗn hợp axit
Ví dụ minh họa
Bài 1: Hòa tan 4,59 gam nhôm trong dung dịch HNO3 1M thu được hỗn hợp X gồm hai khí NO và N2O, tỉ khối hơi của X đối với hidro bằng 16,75. Tính :
a) Thể tích mỗi khí đo ở đktc.
b) Khối lượng muối thu đươc.
c) Thể tích dung dịch HNO3 đã dùng.
Hướng dẫn:
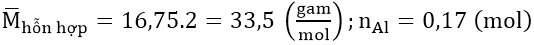
Áp dụng phương pháp sơ đồ chéo:

Gọi nN2O = x (mol) và nNO = 3x (mol)

Áp dụng bảo toàn số mol electron: 17x = 0,51 ⇒ x = 0,03 (mol)
⇒ nNO = 0,09 (mol); nN2O = 0,03 (mol)
a) VNO = 0,09.22,4 = 2,016 (lít); VN2O = 0,03.22,4 = 0,672 (lit)
nHNO3 = nHNO3 bị khử + nHNO3 tham gia tạo muối = 5x + 3.nAl = 0,03 + 3.0,17 = 0,66(mol)
b) mmuối = n_Al.M = 0,17.213 = 36,21 (gam)
c) VHNO3 đã dùng = 0,66/1 = 0,66 (lít)
Bài 2: Cho 11 gam hỗn hợp Al và Fe vào dung dịch HNO3 loãng lấy dư thì có 6,72 lít khí NO bay ra (đktc). Tính khối lượng của mỗi kim loại trong hỗn hợp.
Hướng dẫn:
Gọi số mol Al và Fe trong hỗn hợp là x, y (mol)

Bảo toàn electron: 3x + 3y = 0,9 ⇒ x + y = 0,3 (1)
mhỗn hợp = 27x + 56y = 11 (2)
Giải hệ phương trình (1) và (2): x = 0,2 (mol); y = 0,1 (mol)
Vậy mAl = 5,4 (gam) và mFe = 5,6 (gam)
Bài 3: Cho 3,87 gam hỗn hợp A gồm Mg và Al vào 250 ml dung dịch X chứa axit HCl 1M và H2SO4 0,5M được dung dịch B và 4,368 lít H2 (đktc)
a) Tính phần trăm khối lượng kim loại trong A.
b) Tính thể tích dung dịch C gồm NaOH 0,2M và Ba(OH)2 0,1M cần để trung hòa hết lượng axit dư trong B.
Hướng dẫn:
a) Đối với bài tập có hỗn hợp axit, bazo giải theo phương trình ôn
nHCl = 0,25 (mol) ; nH2SO4 = 0,125 (mol); nH2 = 0,195 (mol)
= nH+ = 0,25 + 2.0,125 = 0,5 (mol);
nH2.2 < nH+ ⇒ H+ dư

Theo đề bài, ta có hệ phương trình:

Giải hệ phương trình ta được: x = 0,06 và y = 0,09
⇒ mMg = 1,44 (gam); mAl = 2,43(gam)
b) Gọi thể tích dung dịch C cần dùng là V (lít)
Ta có: nNaOH = 0,02V(mol); nBa(OH)2 = 0,11V (mol)
⇒ n-OH = 0,2 + 0,2 = 0,4V(mol)
nH+dư = 0,5 - (2x + 3y) = 0,11 (mol)

⇒ 0,11 = 0,4V ⇒ V = 0,275 (lít)
Được cập nhật: 23 tháng 4 lúc 18:17:31 | Lượt xem: 420




